学术动态
张泽民团队《Immunity》揭示SPP1+肿瘤相关巨噬细胞调控肿瘤免疫新机制
作者:楚晓菁 来源自:中国免疫学会 点击数:30031 发布时间:2026-04-28
4月27日,重庆医科大学张泽民院士团队在《Immunity》 期刊在线发表题为“An SPP1-SOCS1 pathway constrains interferon responses in tumor-associated macrophages and shapes an immunosuppressive tumor microenvironment”的研究论文。该研究揭示SPP1作为肿瘤相关巨噬细胞(tumor-associated macrophages, TAMs)关键细胞内调控分子,通过影响TRIM21介导的SOCS1泛素化调控过程抑制IFNγ-STAT1-ISGs抗肿瘤信号通路的持续激活,削弱炎症反应和免疫治疗响应。研究为推动靶向TAMs精准医疗提供了新证据。
TAMs在促进癌症进展和导致治疗耐药性方面具有重要作用。其中以上调SPP1为特征的TAMs与更差的病人预后、血管生成、和肝转移相关,使得SPP1+ TAMs在学术界和免疫治疗领域均获得了广泛关注。而靶向SPP1+ TAMs的治疗却受限于两个重要问题悬而未决。首先,SPP1在TAMs中的具体作用及其调控机制尚不明确。其次,尽管抗SPP1抗体在研究中显示出靶向前景,但迄今为止的临床试验尚未证明其显著疗效。我们仍未可知SPP1是否可作为可行的治疗靶点,以及基于抗体的疗法是否是靶向SPP1+ TAMs的合适策略。
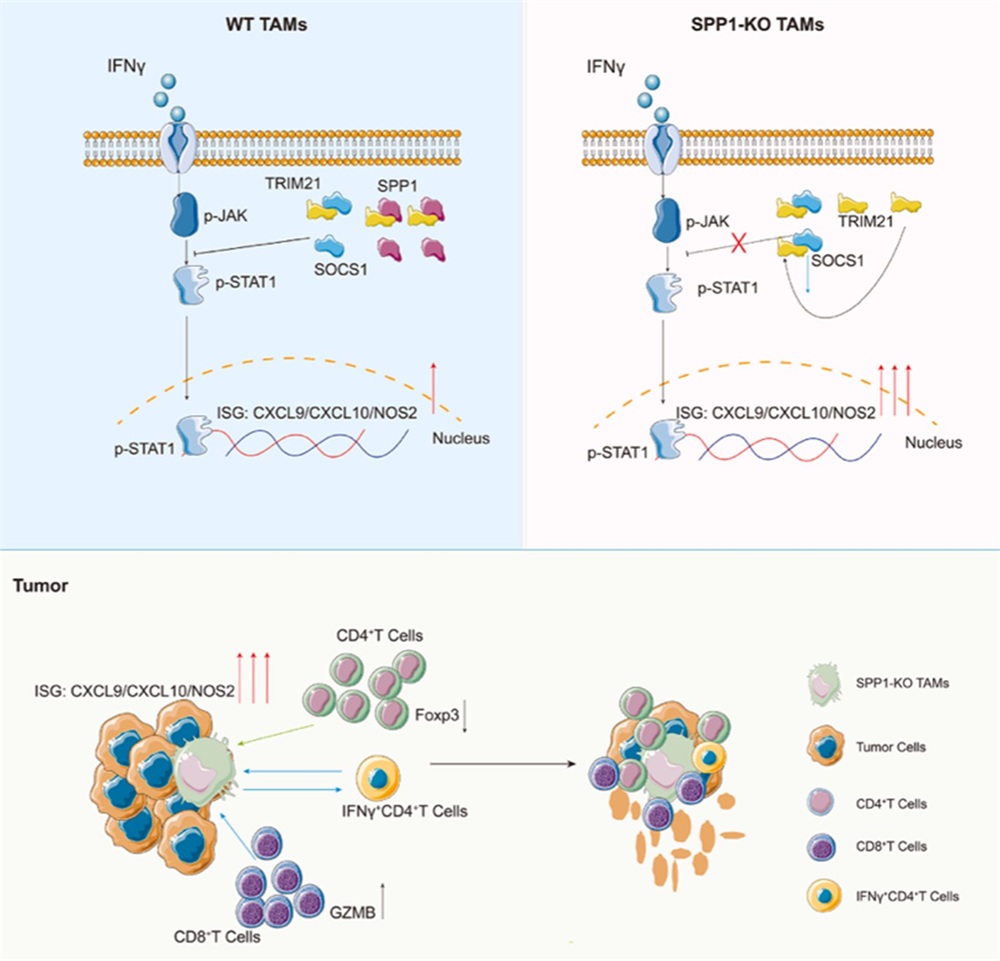
围绕这些问题,研究人员首先通过分析多个癌种的单细胞转录组数据,揭示了SPP1+ TAMs与免疫抑制和免疫检查点阻断(ICB)疗法的耐药性相关。随后通过在TAMs中特异性敲除SPP1,在各种小鼠肿瘤模型中发现了免疫细胞浸润的增加和肿瘤进展的抑制。SPP1敲除的TAMs表现出激活增强的IFNγ-STAT1-ISGs抗肿瘤信号通路,并对肿瘤微环境起到调节作用,发现包括调节性T细胞减少、IFNγ+CD4+ T细胞和GZMB+CD8+ T细胞的增加等现象。
进一步机制研究发现,胞内SPP1的表达受到IL10和TGF-β的调控,并通过影响TRIM21介导的SOCS1泛素化调控过程,维持SOCS1所介导的负反馈抑制,进而限制STAT1信号转导及下游干扰素刺激基因的表达。最后,研究人员利用混合转输和脂质体递送靶向核酸药物等方式,在小鼠体内证明靶向TAMs中的SPP1能够显著提升anti-PD1治疗效果。
综上,该研究揭示了SPP1调控TAMs功能的全新机制,也为靶向TAMs逆转肿瘤免疫治疗耐受提供了新的干预思路,为后续推动针对肿瘤免疫微环境的精准干预,提升实体瘤患者免疫治疗获益提供新的理论依据和治疗方向。
重庆医科大学张泽民院士,北京大学朱琳楠副研究员为本文共同通讯作者,重庆医科大学孙良展副教授,北京师范大学楚晓菁讲师为本文共同第一作者。重庆医科大学孔婷婷、陈曦睿、茹佳宁等对本文亦有贡献。
原文链接:https://www.cell.com/immunity/fulltext/S1074-7613(26)00141-X
TAMs在促进癌症进展和导致治疗耐药性方面具有重要作用。其中以上调SPP1为特征的TAMs与更差的病人预后、血管生成、和肝转移相关,使得SPP1+ TAMs在学术界和免疫治疗领域均获得了广泛关注。而靶向SPP1+ TAMs的治疗却受限于两个重要问题悬而未决。首先,SPP1在TAMs中的具体作用及其调控机制尚不明确。其次,尽管抗SPP1抗体在研究中显示出靶向前景,但迄今为止的临床试验尚未证明其显著疗效。我们仍未可知SPP1是否可作为可行的治疗靶点,以及基于抗体的疗法是否是靶向SPP1+ TAMs的合适策略。
围绕这些问题,研究人员首先通过分析多个癌种的单细胞转录组数据,揭示了SPP1+ TAMs与免疫抑制和免疫检查点阻断(ICB)疗法的耐药性相关。随后通过在TAMs中特异性敲除SPP1,在各种小鼠肿瘤模型中发现了免疫细胞浸润的增加和肿瘤进展的抑制。SPP1敲除的TAMs表现出激活增强的IFNγ-STAT1-ISGs抗肿瘤信号通路,并对肿瘤微环境起到调节作用,发现包括调节性T细胞减少、IFNγ+CD4+ T细胞和GZMB+CD8+ T细胞的增加等现象。
进一步机制研究发现,胞内SPP1的表达受到IL10和TGF-β的调控,并通过影响TRIM21介导的SOCS1泛素化调控过程,维持SOCS1所介导的负反馈抑制,进而限制STAT1信号转导及下游干扰素刺激基因的表达。最后,研究人员利用混合转输和脂质体递送靶向核酸药物等方式,在小鼠体内证明靶向TAMs中的SPP1能够显著提升anti-PD1治疗效果。

综上,该研究揭示了SPP1调控TAMs功能的全新机制,也为靶向TAMs逆转肿瘤免疫治疗耐受提供了新的干预思路,为后续推动针对肿瘤免疫微环境的精准干预,提升实体瘤患者免疫治疗获益提供新的理论依据和治疗方向。
重庆医科大学张泽民院士,北京大学朱琳楠副研究员为本文共同通讯作者,重庆医科大学孙良展副教授,北京师范大学楚晓菁讲师为本文共同第一作者。重庆医科大学孔婷婷、陈曦睿、茹佳宁等对本文亦有贡献。
原文链接:https://www.cell.com/immunity/fulltext/S1074-7613(26)00141-X
