学术动态
阮承超与多位合作者《Nat Immunol》揭示血管外膜淋巴免疫微环境在主动脉瘤发生发展中的作用机制
作者:阮承超 来源自:中国免疫学会 点击数:19480 发布时间:2026-04-16
2026年2月27日,上海交通大学/复旦大学阮承超等在《Nature Immunology》杂志发表题为“Sparcl1 mitigates abdominal aortic aneurysm through inhibiting lymphangiogenesis-mediated TLS formation”的研究论文(封面论文,见下图)。该研究发现血管外膜原位巨噬细胞来源的细胞基质蛋白Sparcl1,通过阻断病理性淋巴管新生,抑制血管外膜三级淋巴样结构(Tertiary Lymphoid Structures, TLS)形成,从而改善高血压诱导的腹主动脉瘤(AAA)的进展。该发现揭示了血管外膜淋巴免疫微环境在动脉瘤发生发展中的作用,并通过设计靶向淋巴循环的治疗性多肽,为开展临床转化研究奠定了理论基础。
血管外膜是一个高度复杂且功能活跃的细胞生态位,远非简单的支撑结构。其核心由具有高度可塑性的外膜成纤维细胞和紧邻的血管周围脂肪细胞组成。此外,血管外膜内常驻着巨噬细胞、T细胞等免疫细胞群体以及神经末梢和滋养血管网络,并在病理早期大量募集更多免疫细胞,使其成为驱动高血压,动脉瘤等血管疾病的慢性炎症灶。然而这些不同细胞间通讯是如何维持或破坏血管稳态仍是亟待解决的关键科学问题。
首先,研究团队分析了来自AAA临床样本和小鼠模型的公共单细胞转录组数据集,发现血管外膜Lyve阳性原位巨噬细胞数量显著减少。研究人员通过构建Lyve1阳性巨噬细胞清除小鼠(Lyve1-Cre; Csf1rflox/flox;LdlrKO),证实血管外膜Lyve1+ 巨噬细胞抑制AAA进展。研究团队结合多组学数据分析发现细胞基质蛋白Sparcl1在AAA组织的血管外膜Lyve1+ 巨噬细胞表达显著降低。通过构建Lyve1+ 巨噬细胞特异Sparcl1敲除小鼠,证实缺失Sparcl1加重血管紧张素II(AngII)诱导的AAA发生发展。
随后,研究人员通过生信分析发现Sparcl1主要参与脉管生成过程的调控。进一步分析发现Sparcl1主要参与调节淋巴管生成。通过染色和成像技术,研究人员发现Sparcl1敲除促进动脉瘤进展过程中血管外膜毛细淋巴管新生,而非集合淋巴管的形成。并通过体内活体成像证实这些新生的毛细淋巴管不具有完整的引流功能,反而大量表达淋巴趋化因子,进而募集大量的T/B淋巴细胞,促进TLS的形成。接下来的机制研究发现Sparcl1通过直接结合FGF2,形成FGF陷阱(FGF-Trap),直接阻断FGF2诱导的病理性淋巴管新生。并通过体外细胞实验和在体的Matrigel实验证实过表达Sparcl1阻断FGF2诱导的淋巴趋化因子的表达。
最后,为了开发基于Sparcl1的新治疗策略,研究人员根据Sparcl1和FGF2的作用位点,设计了新型治疗性多肽Spa17,并通过多肽药物的安全性评价证实其在实验动物体内具有良好的安全性。在此基础上,研究人员利用多种动脉瘤模型,证实Spa17肽能显著抑制血管外膜病理性淋巴管生成,三级淋巴样结构形成和动脉瘤的进展,为进一步开展Spa17多肽的临床前实验奠定了良好的基础。
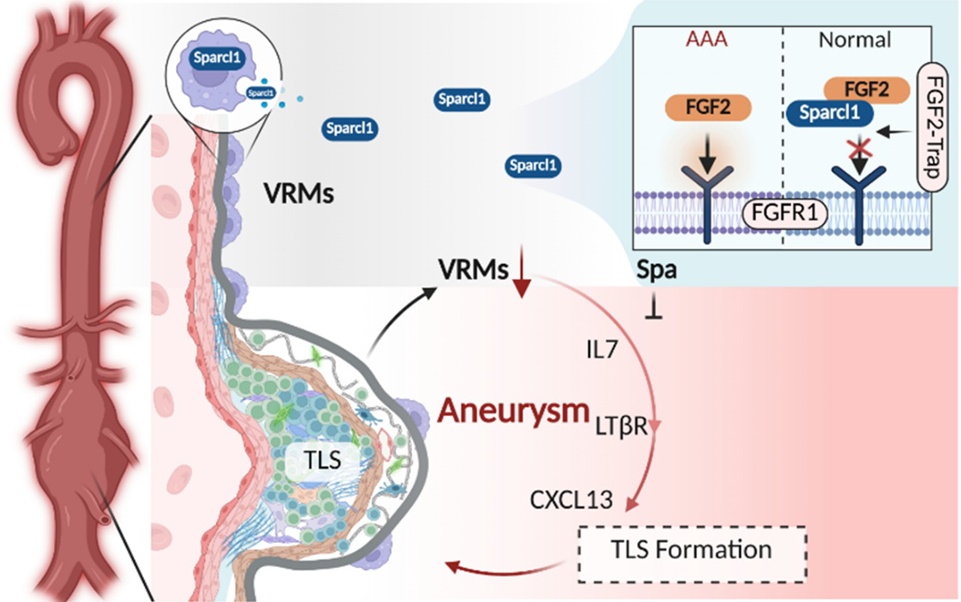
综上,该研究系统阐明了血管外膜组织原位巨噬细胞来源的Sparcl1在动脉瘤中的保护作用,揭示了其通过抑制FGF2驱动的病理性淋巴管生成和三级淋巴样结构形成的分子机制,并开发了具有临床应用前景的治疗性多肽Spa17。
上海交通大学附属第六人民医院陈梅华博士后和复旦大学基础医学院滑艺杰博士为本文第一作者。上海交通大学医学院附属胸科医院阮承超研究员,复旦大学基础医学院庄涛副研究员,上海交通大学医学院附属第六人民医院陆炎研究员,复旦大学附属中山医院董智慧教授和上海交通大学医学院附属瑞金医院卢湾分院李燕医师为本文共同通讯作者。该工作得到了国家自然科学基金,科技部重点研发计划和四大慢病重大专项等项目资助。
原文链接:https://www.nature.com/articles/s41590-026-02454-1

血管外膜是一个高度复杂且功能活跃的细胞生态位,远非简单的支撑结构。其核心由具有高度可塑性的外膜成纤维细胞和紧邻的血管周围脂肪细胞组成。此外,血管外膜内常驻着巨噬细胞、T细胞等免疫细胞群体以及神经末梢和滋养血管网络,并在病理早期大量募集更多免疫细胞,使其成为驱动高血压,动脉瘤等血管疾病的慢性炎症灶。然而这些不同细胞间通讯是如何维持或破坏血管稳态仍是亟待解决的关键科学问题。
首先,研究团队分析了来自AAA临床样本和小鼠模型的公共单细胞转录组数据集,发现血管外膜Lyve阳性原位巨噬细胞数量显著减少。研究人员通过构建Lyve1阳性巨噬细胞清除小鼠(Lyve1-Cre; Csf1rflox/flox;LdlrKO),证实血管外膜Lyve1+ 巨噬细胞抑制AAA进展。研究团队结合多组学数据分析发现细胞基质蛋白Sparcl1在AAA组织的血管外膜Lyve1+ 巨噬细胞表达显著降低。通过构建Lyve1+ 巨噬细胞特异Sparcl1敲除小鼠,证实缺失Sparcl1加重血管紧张素II(AngII)诱导的AAA发生发展。
随后,研究人员通过生信分析发现Sparcl1主要参与脉管生成过程的调控。进一步分析发现Sparcl1主要参与调节淋巴管生成。通过染色和成像技术,研究人员发现Sparcl1敲除促进动脉瘤进展过程中血管外膜毛细淋巴管新生,而非集合淋巴管的形成。并通过体内活体成像证实这些新生的毛细淋巴管不具有完整的引流功能,反而大量表达淋巴趋化因子,进而募集大量的T/B淋巴细胞,促进TLS的形成。接下来的机制研究发现Sparcl1通过直接结合FGF2,形成FGF陷阱(FGF-Trap),直接阻断FGF2诱导的病理性淋巴管新生。并通过体外细胞实验和在体的Matrigel实验证实过表达Sparcl1阻断FGF2诱导的淋巴趋化因子的表达。
最后,为了开发基于Sparcl1的新治疗策略,研究人员根据Sparcl1和FGF2的作用位点,设计了新型治疗性多肽Spa17,并通过多肽药物的安全性评价证实其在实验动物体内具有良好的安全性。在此基础上,研究人员利用多种动脉瘤模型,证实Spa17肽能显著抑制血管外膜病理性淋巴管生成,三级淋巴样结构形成和动脉瘤的进展,为进一步开展Spa17多肽的临床前实验奠定了良好的基础。

综上,该研究系统阐明了血管外膜组织原位巨噬细胞来源的Sparcl1在动脉瘤中的保护作用,揭示了其通过抑制FGF2驱动的病理性淋巴管生成和三级淋巴样结构形成的分子机制,并开发了具有临床应用前景的治疗性多肽Spa17。
上海交通大学附属第六人民医院陈梅华博士后和复旦大学基础医学院滑艺杰博士为本文第一作者。上海交通大学医学院附属胸科医院阮承超研究员,复旦大学基础医学院庄涛副研究员,上海交通大学医学院附属第六人民医院陆炎研究员,复旦大学附属中山医院董智慧教授和上海交通大学医学院附属瑞金医院卢湾分院李燕医师为本文共同通讯作者。该工作得到了国家自然科学基金,科技部重点研发计划和四大慢病重大专项等项目资助。
原文链接:https://www.nature.com/articles/s41590-026-02454-1
