学术动态
王广川/陈洛南/景乃禾团队开发CLIM-TIME技术解析转移瘤免疫治疗抵抗的关键机制
作者:王英华 来源自:中国免疫学会 点击数:10163 发布时间:2026-03-17
2026年2月12日,中国科学院分子细胞科学卓越创新中心王广川/陈洛南团队及广州国家实验室的景乃禾团队在《Cell》期刊发表题为“CLIM-TIME identifies metastatic microenvironment modulators for T cell therapy response”的研究论文。该研究开发了一种新型微环境空间扰动筛选平台——CLIM-TIME(CRISPR-Laser-captured microdissection Integration Mapping of Tumor Immune Microenvironment),不仅系统揭示了肿瘤内在突变与肺转移微环境空间结构及免疫治疗应答之间的因果联系,还鉴定出重塑转移灶微环境来提升T细胞浸润及治疗疗效的关键靶点。
肿瘤转移是导致癌症患者死亡的主要原因之一。转移过程中形成的肿瘤微环境为肿瘤细胞提供了生存和扩增所需的关键生态条件。近年来的研究表明,转移瘤微环境的组成和结构特征与免疫治疗疗效密切相关。然而,对于“肿瘤内在遗传改变如何驱动特定免疫微环境的形成,并进一步影响免疫治疗应答”的系统性认识仍然不足,相关研究技术和分析方法仍有待进一步发展。
研究团队依托 CLIM-TIME 技术平台,系统评估抑癌基因缺失对转移瘤微环境及免疫治疗响应的影响。研究者构建了覆盖391种常见抑癌基因缺失的文库肿瘤模型,并对其形成的肺转移灶开展多维度分析,包括转录组特征、免疫细胞空间分布、免疫逃逸能力以及T细胞治疗应答等。综合分析显示,不同基因驱动的转移瘤可形成七种具有代表性的微环境类型,并呈现出明显差异的转录组特征。
研究发现,其中一类对T细胞治疗耐受的转移瘤微环境状态:“髓系细胞富集且T细胞排斥型(T-IE/M-II)”,其特征表现显著富集细胞外基质(ECM)重塑相关通路,包括胶原沉积及细胞黏着斑激酶(FAK)信号通路,提示基质结构变化可能在T细胞排斥中发挥关键作用。
进一步研究表明,Hippo 信号通路中多个抑癌基因的缺失倾向于驱动形成 T-IE/M-II 型微环境,并导致T细胞治疗耐受。以 Nf2 缺失为代表的模型显示,相关转移灶中T细胞浸润显著减少,而髓系细胞浸润增加,并伴随胶原沉积增强。机制研究发现,Nf2 缺失的肿瘤细胞上调多种ECM相关基因的表达,包括胶原交联酶 LOXL2,并进一步诱导募集的髓系细胞表达基质相关基因并呈现“M2”样免疫抑制表型,从而共同促进T细胞排斥和功能耗竭。
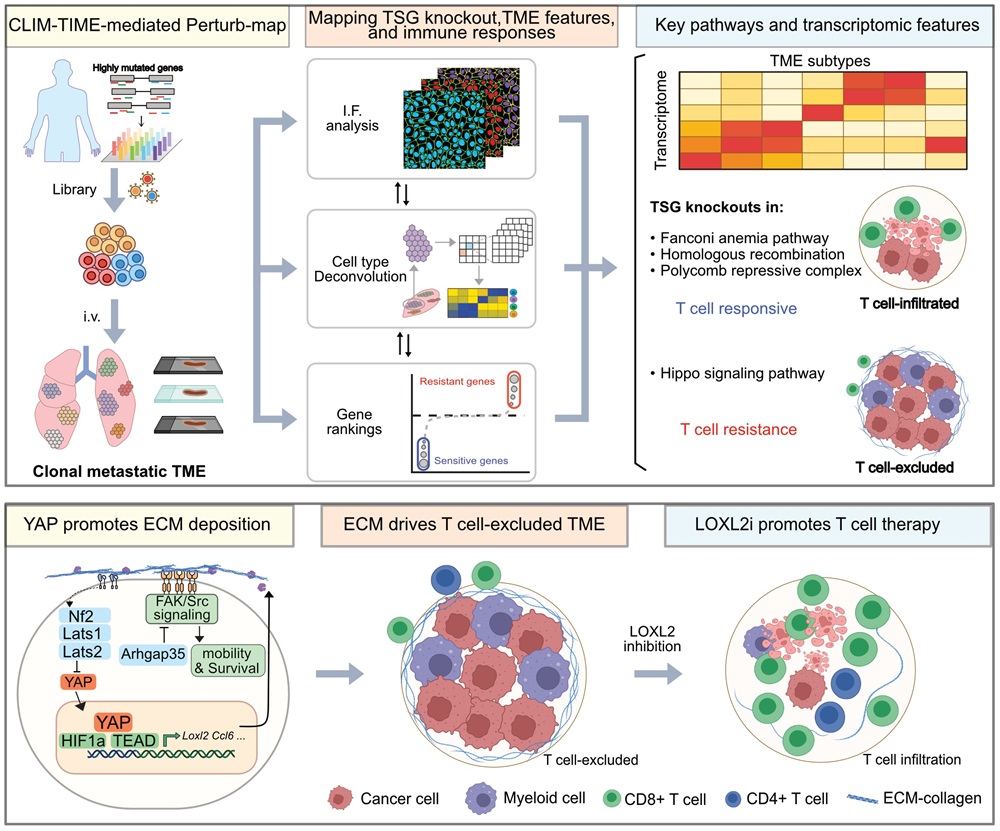
临床数据分析显示,LOXL2 高表达与转移瘤中T细胞浸润降低及免疫治疗反应不佳显著相关。功能实验表明,敲除 LOXL2 或抑制其酶活性可减少胶原沉积、降低髓系细胞浸润并增加T细胞进入肿瘤,从而使原本对T细胞治疗不敏感的转移瘤转变为治疗响应型。在多种小鼠及人源转移瘤模型中,靶向抑制 LOXL2 均可显著增强 TCR-T 和 CAR-T 细胞治疗效果。
该研究在高通量尺度上建立了“肿瘤内在遗传改变—微环境结构—免疫治疗疗效”之间的因果联系,并结合机器学习筛选出决定转移瘤免疫状态的关键基因,构建了更精准的免疫治疗应答预测模型,为克服转移瘤免疫治疗耐药提供了新的研究思路和潜在干预靶点。
原文链接:https://www.sciencedirect.com/science/article/pii/S0092867425014916
肿瘤转移是导致癌症患者死亡的主要原因之一。转移过程中形成的肿瘤微环境为肿瘤细胞提供了生存和扩增所需的关键生态条件。近年来的研究表明,转移瘤微环境的组成和结构特征与免疫治疗疗效密切相关。然而,对于“肿瘤内在遗传改变如何驱动特定免疫微环境的形成,并进一步影响免疫治疗应答”的系统性认识仍然不足,相关研究技术和分析方法仍有待进一步发展。
研究团队依托 CLIM-TIME 技术平台,系统评估抑癌基因缺失对转移瘤微环境及免疫治疗响应的影响。研究者构建了覆盖391种常见抑癌基因缺失的文库肿瘤模型,并对其形成的肺转移灶开展多维度分析,包括转录组特征、免疫细胞空间分布、免疫逃逸能力以及T细胞治疗应答等。综合分析显示,不同基因驱动的转移瘤可形成七种具有代表性的微环境类型,并呈现出明显差异的转录组特征。
研究发现,其中一类对T细胞治疗耐受的转移瘤微环境状态:“髓系细胞富集且T细胞排斥型(T-IE/M-II)”,其特征表现显著富集细胞外基质(ECM)重塑相关通路,包括胶原沉积及细胞黏着斑激酶(FAK)信号通路,提示基质结构变化可能在T细胞排斥中发挥关键作用。
进一步研究表明,Hippo 信号通路中多个抑癌基因的缺失倾向于驱动形成 T-IE/M-II 型微环境,并导致T细胞治疗耐受。以 Nf2 缺失为代表的模型显示,相关转移灶中T细胞浸润显著减少,而髓系细胞浸润增加,并伴随胶原沉积增强。机制研究发现,Nf2 缺失的肿瘤细胞上调多种ECM相关基因的表达,包括胶原交联酶 LOXL2,并进一步诱导募集的髓系细胞表达基质相关基因并呈现“M2”样免疫抑制表型,从而共同促进T细胞排斥和功能耗竭。

临床数据分析显示,LOXL2 高表达与转移瘤中T细胞浸润降低及免疫治疗反应不佳显著相关。功能实验表明,敲除 LOXL2 或抑制其酶活性可减少胶原沉积、降低髓系细胞浸润并增加T细胞进入肿瘤,从而使原本对T细胞治疗不敏感的转移瘤转变为治疗响应型。在多种小鼠及人源转移瘤模型中,靶向抑制 LOXL2 均可显著增强 TCR-T 和 CAR-T 细胞治疗效果。
该研究在高通量尺度上建立了“肿瘤内在遗传改变—微环境结构—免疫治疗疗效”之间的因果联系,并结合机器学习筛选出决定转移瘤免疫状态的关键基因,构建了更精准的免疫治疗应答预测模型,为克服转移瘤免疫治疗耐药提供了新的研究思路和潜在干预靶点。
原文链接:https://www.sciencedirect.com/science/article/pii/S0092867425014916
