学术动态
王伊龙/张明君团队《Cell》开创颅骨骨髓免疫细胞介导脑靶向递药新策略
作者:郑赟、陈壮壮 来源自:中国免疫学会 点击数:9056 发布时间:2026-03-16
2026年3月5日,首都医科大学附属北京天坛医院王伊龙教授团队与清华大学张明君教授团队在《Cell》期刊发表题为“Nanoparticles hijack calvarial immune cells for CNS drug delivery and stroke therapy”的研究论文。该研究创新性提出一种利用颅骨骨髓免疫细胞负载纳米药物,实现中枢神经系统靶向递药的新策略:研究团队通过颅骨骨髓注射(intracalvariosseous, ICO)将药物负载纳米颗粒递送至颅骨骨髓,使其被局部髓系免疫细胞摄取,并借助颅骨—脑膜微通道(skull–meninges channel, SMC)迁移进入脑组织,从而绕过血脑屏障,实现脑卒中的高效精准治疗。
中枢神经系统疾病的药物研发长期受到血脑屏障(blood–brain barrier, BBB)的限制,大多数药物难以有效到达脑部病变区域。尽管纳米载体递送和免疫细胞递送等策略不断被探索,但仍面临靶向性不足、系统暴露风险高及临床转化困难等问题。近年来研究发现,颅骨骨髓作为脑膜邻近的重要免疫枢纽,通过SMC与脑膜直接连通,在中枢神经系统炎症或损伤时能够快速向脑组织募集免疫细胞。这一独特的解剖与免疫学特征,为绕过血脑屏障实现脑部药物递送提供了新的可能。
在本研究中,研究团队构建了具有髓系细胞亲和性的白蛋白纳米颗粒,并通过ICO注射将其递送至小鼠颅骨骨髓。体内实验结果表明,这些纳米颗粒能够被颅骨骨髓中的Gr1⁺髓系细胞高效吞噬,并在神经炎症状态下表现出更高的摄取效率,提示在疾病条件下免疫细胞具有更强的药物负载能力。
通过颅骨透明化成像及免疫荧光分析发现,在中枢神经系统炎症条件下,大量负载纳米颗粒的髓系细胞能够沿SMC向脑膜区域迁移,并在硬脑膜区域广泛分布。透射电镜观察进一步证实纳米颗粒位于迁移髓系细胞胞内,提示颅骨骨髓免疫细胞可作为“天然递药载体”,将药物经此通道运输至中枢神经系统边界。
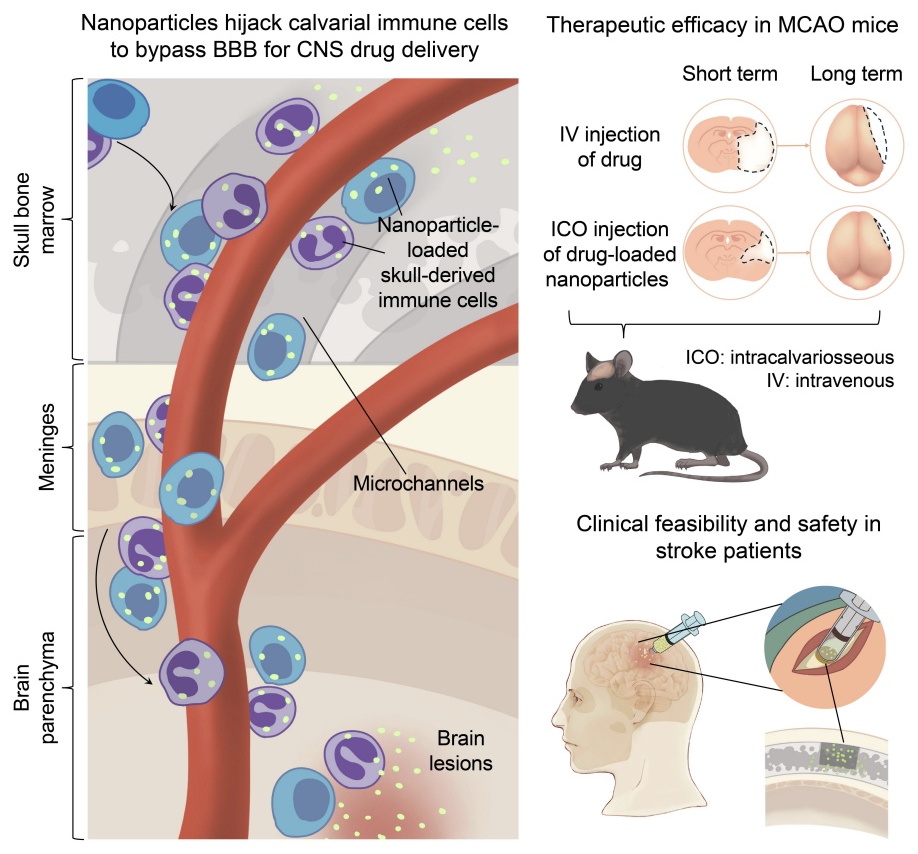
在脑卒中动物模型中,研究团队发现负载纳米颗粒的髓系细胞能够进一步向脑损伤区域聚集,从而显著提高药物在脑病灶部位的蓄积效率。与传统静脉给药方式相比,该递药策略能够大幅减少用药剂量(仅为静脉剂量的1/15),更有效地实现脑部靶向递送,并在动物模型中改善神经功能结局,为后续临床应用奠定了实验基础。
为进一步评估该策略的临床转化潜力,研究团队开展了一项前瞻性、随机、开放标签的临床试验——SOLUTION(NCT05849805),用于评估ICO在恶性大脑中动脉梗死(malignant middle cerebral artery infarction, mMCAI)患者中的安全性与可行性。研究结果显示,颅骨内注射操作简便,平均手术时间约30分钟,所有受试者均未出现严重并发症。相关真实世界数据初步证实了该策略在临床中的可行性与安全性,提示该方案具备较强的临床转化基础。
综上所述,该研究系统揭示并验证了一种基于“颅骨骨髓免疫细胞—脑膜微通道”的新型药物递送机制,通过“劫持”颅骨骨髓免疫细胞作为药物载体,实现绕过血脑屏障的脑靶向递药,为中枢神经系统疾病治疗提供了新的技术路径,也为脑卒中及其 他神经系统疾病的精准治疗提供了重要的理论基础和潜在的转化医学策略。
清华大学博士研究生高喜泽、首都医科大学附属北京天坛医院刘向荣研究员及博士后王楠星为该论文的共同第一作者。该研究得到国家自然科学基金、首都医学科学创新中心等项目的资助。
原文链接:https://www.cell.com/cell/fulltext/S0092-8674(25)01421-7
中枢神经系统疾病的药物研发长期受到血脑屏障(blood–brain barrier, BBB)的限制,大多数药物难以有效到达脑部病变区域。尽管纳米载体递送和免疫细胞递送等策略不断被探索,但仍面临靶向性不足、系统暴露风险高及临床转化困难等问题。近年来研究发现,颅骨骨髓作为脑膜邻近的重要免疫枢纽,通过SMC与脑膜直接连通,在中枢神经系统炎症或损伤时能够快速向脑组织募集免疫细胞。这一独特的解剖与免疫学特征,为绕过血脑屏障实现脑部药物递送提供了新的可能。
在本研究中,研究团队构建了具有髓系细胞亲和性的白蛋白纳米颗粒,并通过ICO注射将其递送至小鼠颅骨骨髓。体内实验结果表明,这些纳米颗粒能够被颅骨骨髓中的Gr1⁺髓系细胞高效吞噬,并在神经炎症状态下表现出更高的摄取效率,提示在疾病条件下免疫细胞具有更强的药物负载能力。
通过颅骨透明化成像及免疫荧光分析发现,在中枢神经系统炎症条件下,大量负载纳米颗粒的髓系细胞能够沿SMC向脑膜区域迁移,并在硬脑膜区域广泛分布。透射电镜观察进一步证实纳米颗粒位于迁移髓系细胞胞内,提示颅骨骨髓免疫细胞可作为“天然递药载体”,将药物经此通道运输至中枢神经系统边界。

在脑卒中动物模型中,研究团队发现负载纳米颗粒的髓系细胞能够进一步向脑损伤区域聚集,从而显著提高药物在脑病灶部位的蓄积效率。与传统静脉给药方式相比,该递药策略能够大幅减少用药剂量(仅为静脉剂量的1/15),更有效地实现脑部靶向递送,并在动物模型中改善神经功能结局,为后续临床应用奠定了实验基础。
为进一步评估该策略的临床转化潜力,研究团队开展了一项前瞻性、随机、开放标签的临床试验——SOLUTION(NCT05849805),用于评估ICO在恶性大脑中动脉梗死(malignant middle cerebral artery infarction, mMCAI)患者中的安全性与可行性。研究结果显示,颅骨内注射操作简便,平均手术时间约30分钟,所有受试者均未出现严重并发症。相关真实世界数据初步证实了该策略在临床中的可行性与安全性,提示该方案具备较强的临床转化基础。
综上所述,该研究系统揭示并验证了一种基于“颅骨骨髓免疫细胞—脑膜微通道”的新型药物递送机制,通过“劫持”颅骨骨髓免疫细胞作为药物载体,实现绕过血脑屏障的脑靶向递药,为中枢神经系统疾病治疗提供了新的技术路径,也为脑卒中及其 他神经系统疾病的精准治疗提供了重要的理论基础和潜在的转化医学策略。
清华大学博士研究生高喜泽、首都医科大学附属北京天坛医院刘向荣研究员及博士后王楠星为该论文的共同第一作者。该研究得到国家自然科学基金、首都医学科学创新中心等项目的资助。
原文链接:https://www.cell.com/cell/fulltext/S0092-8674(25)01421-7
