学术动态
吕凌团队《Cell》揭示肿瘤来源氨重编程Treg代谢驱动免疫抑制机制
作者:古鉴 来源自:中国免疫学会 点击数:7905 发布时间:2026-02-28
在肿瘤免疫治疗中,调节性T细胞(Treg)在肿瘤微环境中的持续富集和功能增强,是导致免疫检查点抑制剂(ICB)疗效受限及耐药的重要因素。如何从代谢层面揭示Treg在肿瘤微环境中的适应机制,并寻找可干预的关键节点,是当前肿瘤免疫领域的重要科学问题。解决这一问题的核心在于系统解析肿瘤代谢重塑与免疫抑制网络之间的内在联系及其关键调控轴。
2026年1月22日,徐州医科大学附属医院与南京医科大学第一附属医院吕凌教授、古鉴教授及团队在国际顶级学术期刊《Cell》发表题为“Tumor-produced ammonia is metabolized by regulatory T cells to further impede anti-tumor immunity” 的研究论文。该研究通过空间多组学整合分析、代谢示踪、结构生物学及多种体内外功能模型,系统揭示了肿瘤来源氨在塑造免疫抑制微环境中的关键作用,并首次阐明调节性T细胞通过代谢重编程主动利用氨,从而增强自身稳定性和免疫抑制功能的分子机制。这一发现为理解肿瘤代谢与免疫耐受之间的耦联关系提供了新的理论框架。
肿瘤细胞高度活跃的谷氨酰胺分解代谢伴随大量氨的产生。既往研究表明,氨可诱导CD8⁺效T细胞凋亡或功能衰竭,但Treg却在高氨区域持续富集。研究团队通过人肝癌空间多组学分析发现,在高谷氨酰胺分解且尿素循环活性低下的肿瘤区域,Treg显著聚集而效应T细胞减少。进一步证实,驱动这一现象的关键并非谷氨酰胺代谢本身,而是其副产物—氨的局部积累。
机制上,Treg具有两条特异性的氨适应通路。一方面,氨通过SRC3-STAT3轴上调ASL,激活尿素循环清除胞内氨,维持细胞稳态;而效应T细胞缺乏这一应答,更易受损。另一方面,氨刺激下FOXP3上调SMS,促进精胺生成。精胺直接结合PPARγ并增强其转录活性,上调线粒体呼吸链基因,增强氧化磷酸化水平,从而显著提升Treg抑制功能。PPARγ突变实验进一步确认,“FOXP3-SMS-精胺-PPARγ”轴是Treg代谢重编程的核心机制。
研究还进一步揭示了氨在免疫治疗耐药中的潜在作用。在抗PD-1治疗过程中,肿瘤细胞死亡可通过联合脱氨基释放大量氨,导致肿瘤局部氨水平升高,继而强化Treg功能并促进免疫耐药。动物模型证实,抑制GLUD1可有效降低治疗后肿瘤组织中的氨水平,减少Treg浸润,并显著增强PD-1治疗效果。这一发现提示,单纯抑制谷氨酰胺代谢不足以完全控制氨的产生,靶向脱氨途径或直接调控氨清除策略,可能成为克服免疫耐药的重要方向。
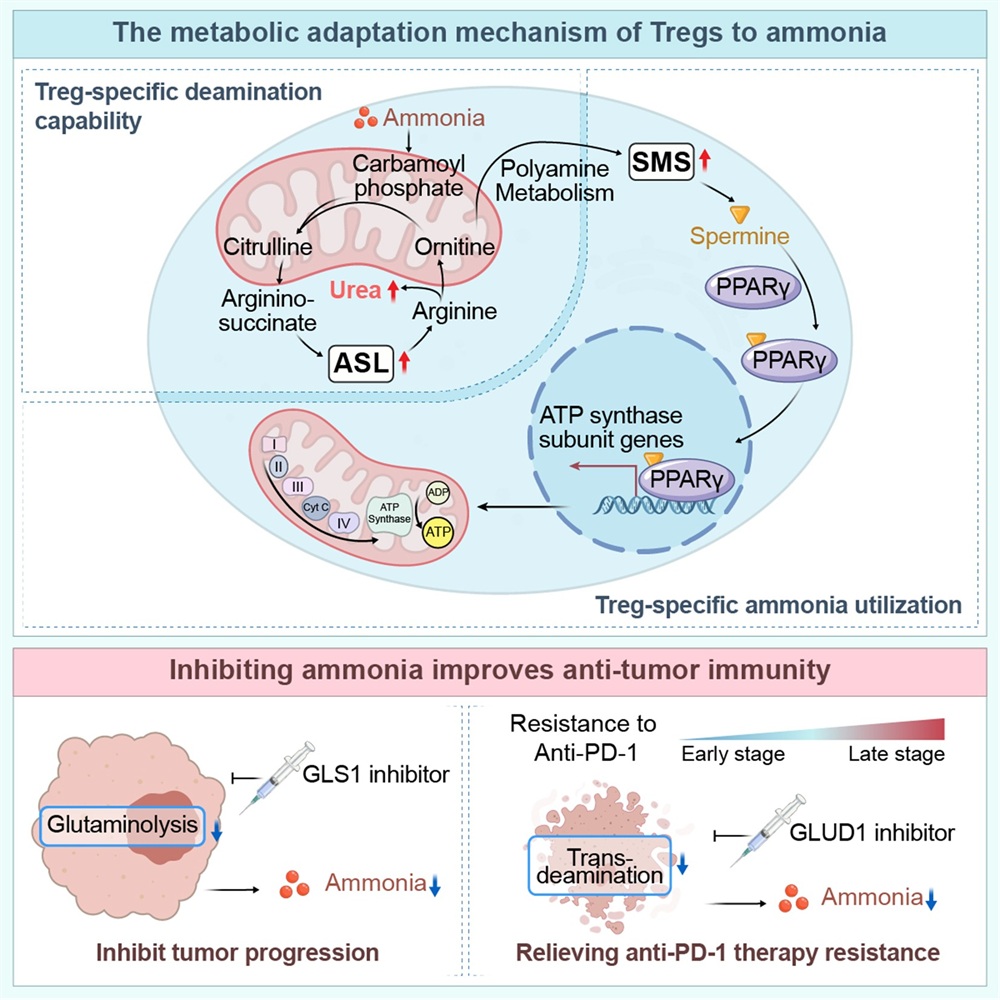
综上所述,该研究系统阐明了肿瘤来源氨通过两条Treg特异性代谢通路——SRC3/STAT3-ASL驱动的尿素循环解毒通路以及FOXP3-SMS-精胺-PPARγ代谢强化轴——促进Treg存活与功能增强的分子机制,揭示了肿瘤代谢副产物在塑造免疫抑制微环境中的决定性作用。该成果不仅加深了对Treg代谢适应机制的理解,也为开发以氨代谢为靶点的联合免疫治疗策略提供了新的理论依据和潜在靶点。
吕凌教授为该论文的主要通讯作者,古鉴教授为该论文的并列通讯作者兼第一作者,李彧博士、陈秋阳博士、宋子延及钱去非为共同第一作者。该研究获得国家自然科学基金、国家重点研发计划及江苏省相关科研项目的支持。
原文链接:https://www.sciencedirect.com/science/article/pii/S0092867425013698
2026年1月22日,徐州医科大学附属医院与南京医科大学第一附属医院吕凌教授、古鉴教授及团队在国际顶级学术期刊《Cell》发表题为“Tumor-produced ammonia is metabolized by regulatory T cells to further impede anti-tumor immunity” 的研究论文。该研究通过空间多组学整合分析、代谢示踪、结构生物学及多种体内外功能模型,系统揭示了肿瘤来源氨在塑造免疫抑制微环境中的关键作用,并首次阐明调节性T细胞通过代谢重编程主动利用氨,从而增强自身稳定性和免疫抑制功能的分子机制。这一发现为理解肿瘤代谢与免疫耐受之间的耦联关系提供了新的理论框架。
肿瘤细胞高度活跃的谷氨酰胺分解代谢伴随大量氨的产生。既往研究表明,氨可诱导CD8⁺效T细胞凋亡或功能衰竭,但Treg却在高氨区域持续富集。研究团队通过人肝癌空间多组学分析发现,在高谷氨酰胺分解且尿素循环活性低下的肿瘤区域,Treg显著聚集而效应T细胞减少。进一步证实,驱动这一现象的关键并非谷氨酰胺代谢本身,而是其副产物—氨的局部积累。
机制上,Treg具有两条特异性的氨适应通路。一方面,氨通过SRC3-STAT3轴上调ASL,激活尿素循环清除胞内氨,维持细胞稳态;而效应T细胞缺乏这一应答,更易受损。另一方面,氨刺激下FOXP3上调SMS,促进精胺生成。精胺直接结合PPARγ并增强其转录活性,上调线粒体呼吸链基因,增强氧化磷酸化水平,从而显著提升Treg抑制功能。PPARγ突变实验进一步确认,“FOXP3-SMS-精胺-PPARγ”轴是Treg代谢重编程的核心机制。
研究还进一步揭示了氨在免疫治疗耐药中的潜在作用。在抗PD-1治疗过程中,肿瘤细胞死亡可通过联合脱氨基释放大量氨,导致肿瘤局部氨水平升高,继而强化Treg功能并促进免疫耐药。动物模型证实,抑制GLUD1可有效降低治疗后肿瘤组织中的氨水平,减少Treg浸润,并显著增强PD-1治疗效果。这一发现提示,单纯抑制谷氨酰胺代谢不足以完全控制氨的产生,靶向脱氨途径或直接调控氨清除策略,可能成为克服免疫耐药的重要方向。

综上所述,该研究系统阐明了肿瘤来源氨通过两条Treg特异性代谢通路——SRC3/STAT3-ASL驱动的尿素循环解毒通路以及FOXP3-SMS-精胺-PPARγ代谢强化轴——促进Treg存活与功能增强的分子机制,揭示了肿瘤代谢副产物在塑造免疫抑制微环境中的决定性作用。该成果不仅加深了对Treg代谢适应机制的理解,也为开发以氨代谢为靶点的联合免疫治疗策略提供了新的理论依据和潜在靶点。
吕凌教授为该论文的主要通讯作者,古鉴教授为该论文的并列通讯作者兼第一作者,李彧博士、陈秋阳博士、宋子延及钱去非为共同第一作者。该研究获得国家自然科学基金、国家重点研发计划及江苏省相关科研项目的支持。
原文链接:https://www.sciencedirect.com/science/article/pii/S0092867425013698
