学术动态
李汉杰团队《Cell》揭示与体型大小有关的外周神经系统小胶质细胞
作者:孙华 来源自:中国免疫学会 点击数:18441 发布时间:2025-04-09
小胶质细胞(microglia)是中枢神经系统(CNS)特异的巨噬细胞,广泛参与神经发育、突触修剪及免疫调控等关键生理过程。自1919年被发现以来,小胶质细胞一直被认为仅存在于中枢神经系统中。基于常见啮齿动物模型的研究结果也显示小胶质细胞只分布在CNS中,而不存在于外周神经系统(PNS)中。2025年4月7日,中国科学院深圳先进技术研究院李汉杰团队在《Cell》期刊发表题为“Peripheral nervous system microglia-like cells regulate neuronal soma size throughout evolution”的研究论文,首次在外周神经系统中发现一类与中枢小胶质细胞分子特征高度相似的新型免疫细胞类群——外周神经系统小胶质细胞(PNS microglia),并揭示其在外周神经元胞体增大、轴突生长及功能成熟中的核心作用。该研究为神经-免疫互作研究提供了全新的视角。

主要发现
跨物种单细胞测序分析揭示PNS microglia的存在
通过对人、食蟹猴、猪、小鼠、大鼠五个物种的中枢与外周神经系统免疫细胞进行单细胞转录组测序,研究团队发现人、食蟹猴、猪的背根神经节中存在一类转录组与CNS小胶质细胞高度相似的细胞类群(PNS microglia),且表达经典小胶质细胞标志基因(如P2RY12、TMEM119、SALL1)。进一步的研究揭示该群细胞在表观组、特征蛋白表达以及个体发育上与中枢小胶质细胞的相似性,因此将其命名为外周神经系统小胶质细胞(PNS microglia)。值得注意的是,小鼠和大鼠外周神经系统中并未检测到此类细胞,这解释了其长期未被发现的可能原因。
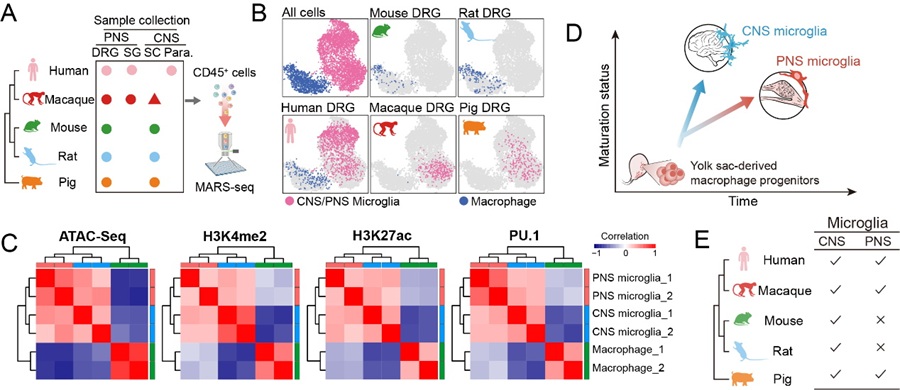
图1. PNS microglia和CNS microglia 具有相同的转录组、表观组及发育路径
PNS类小胶质细胞直接包裹外周神经元胞体,形成“神经元-小胶质细胞-卫星胶质细胞”三元结构
传统教科书认为,外周神经元胞体仅由卫星胶质细胞(SGCs)包裹形成神经元-卫星胶质细胞二元结构。本研究通过高分辨率成像和3D重建技术发现,PNS小胶质细胞主要分布于SGCs形成的包膜内部,直接接触并包裹神经元胞体,形成独特的神经元-PNS小胶质细胞-卫星胶质细胞三元结构。这一空间定位模式在人类、猴及猪的外周神经节中高度保守。这一发现不仅修正了传统模型,还提示三者间很可能存在密切的功能互作。
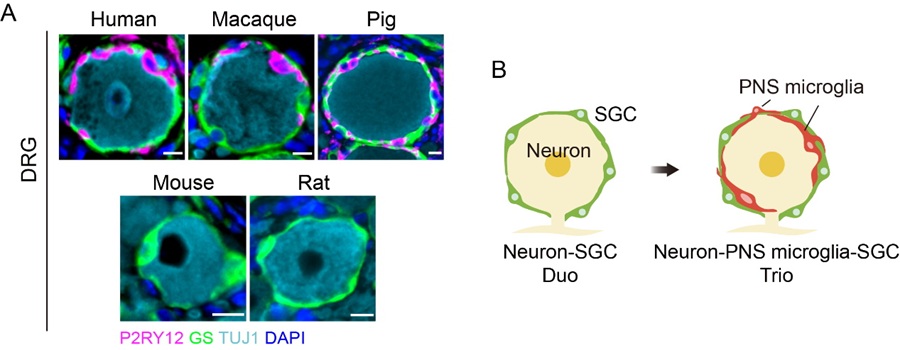
图2. PNS microglia直接包裹外周神经元胞体
PNS microglia调控神经元胞体增大与功能成熟
研究人员利用猪的体内模型清除PNS小胶质细胞后,发现背根神经节(DRG)神经元胞体增大受阻,表皮神经纤维分布明显减少,且对机械刺激的反应显著减弱,表明了PNS小胶质细胞在调控外周神经元发育与功能成熟过程中的重要作用。
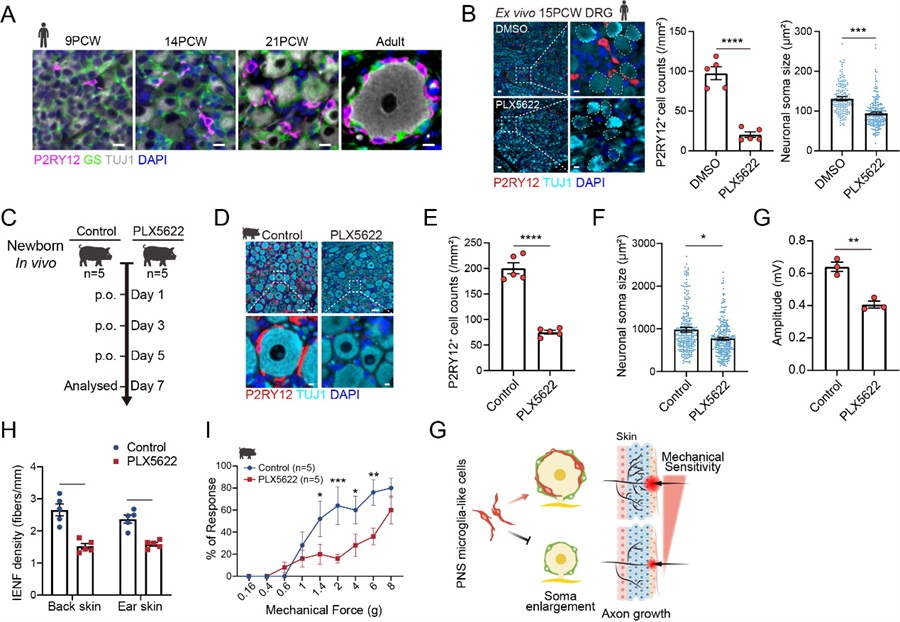
图3. PNS microglia是外周神经元胞体变大,轴突生长,功能成熟所需要的
进化关联:PNS小胶质细胞丰度与物种体型/神经元胞体大小正相关
通过对24种脊椎动物(涵盖鱼类、两栖类、爬行类及哺乳类)进行系统演化分析,团队发现PNS小胶质细胞起源古老,在鱼类、两栖类和爬行类的背根神经节中就已存在。有趣的是,PNS小胶质细胞的丰度与物种的体型大小以及外周神经元胞体大小成正相关,即物种体型越大,外周神经元胞体越大,PNS小胶质细胞的丰度越高,而体型越小的物种,胞体越小,PNS 小胶质细胞越罕见或不存在。这也从侧面证明了PNS小胶质细胞具有调控神经元胞体生长的功能。
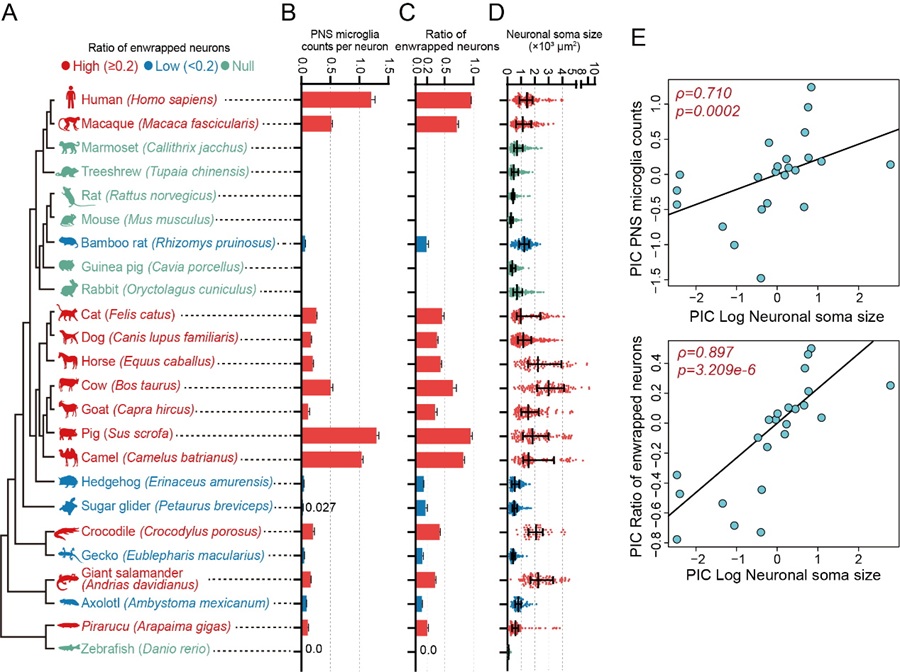
图4. PNS microglia在进化上古老且与物种体型/神经元胞体大小正相关
科学意义
PNS小胶质细胞的发现打破了过去一直认为的“小胶质细胞不存在于外周神经系统”的经典认知。该发现不仅提出了新的免疫-神经互作模式,也拓展了我们对小胶质细胞分布和功能的理解,有望为外周神经系统的发育以及疾病的发生发展研究提供新的视角。
通讯作者简介
李汉杰,国家杰青,重点研发计划首席科学家,中国科学院深圳先进技术研究院研究员。课题组采用“数据和假说双驱动”的研究范式,利用计算生物学,分子细胞生物学,临床样本和动物模型,深入探究人体免疫细胞在生理及病理状态下的发育分化与功能。以通讯或第一作者(含共同)发表多篇高水平论文,包括Cell 3篇(2025,2023,2019)、Cell Research(2020,2012)、Cell Reports Medicine(2024)、Cellular and Molecular Immunology、Cell Discovery、Cell Reports等期刊,总引用超4600次。成果入选2023年国内十大科技新闻(科技日报),2023年深圳市科技创新十件大事(深圳特区报)。曾荣获中组部“海外高层次人才青年项目”、欧盟“玛丽-居里奖学金”、德国“洪堡学者”。作为首席科学家,主持科技部重点研发计划“发育编程及其代谢调节”重点专项。
致谢与资助
中国科学院深圳先进技术研究院吴志生、王毅恒、陈巍魏、孙华及深圳市宝安区妇幼保健院陈晓燕博士为共同第一作者。感谢国家自然科学基金(32425024)、科技部重点研发计划(2020YFA0804100)、深圳市医学科学院专项基金(B2302006)等支持。
原文链接:https://doi.org/10.1016/j.cell.2025.02.007
课题组招聘
实验室长期招收计算生物学、分子细胞生物学、免疫学、基础医学研究员/研究生/博士后,欢迎有志之士前来咨询并加入我们的研究团队。

主要发现
跨物种单细胞测序分析揭示PNS microglia的存在
通过对人、食蟹猴、猪、小鼠、大鼠五个物种的中枢与外周神经系统免疫细胞进行单细胞转录组测序,研究团队发现人、食蟹猴、猪的背根神经节中存在一类转录组与CNS小胶质细胞高度相似的细胞类群(PNS microglia),且表达经典小胶质细胞标志基因(如P2RY12、TMEM119、SALL1)。进一步的研究揭示该群细胞在表观组、特征蛋白表达以及个体发育上与中枢小胶质细胞的相似性,因此将其命名为外周神经系统小胶质细胞(PNS microglia)。值得注意的是,小鼠和大鼠外周神经系统中并未检测到此类细胞,这解释了其长期未被发现的可能原因。

图1. PNS microglia和CNS microglia 具有相同的转录组、表观组及发育路径
PNS类小胶质细胞直接包裹外周神经元胞体,形成“神经元-小胶质细胞-卫星胶质细胞”三元结构
传统教科书认为,外周神经元胞体仅由卫星胶质细胞(SGCs)包裹形成神经元-卫星胶质细胞二元结构。本研究通过高分辨率成像和3D重建技术发现,PNS小胶质细胞主要分布于SGCs形成的包膜内部,直接接触并包裹神经元胞体,形成独特的神经元-PNS小胶质细胞-卫星胶质细胞三元结构。这一空间定位模式在人类、猴及猪的外周神经节中高度保守。这一发现不仅修正了传统模型,还提示三者间很可能存在密切的功能互作。

图2. PNS microglia直接包裹外周神经元胞体
PNS microglia调控神经元胞体增大与功能成熟
研究人员利用猪的体内模型清除PNS小胶质细胞后,发现背根神经节(DRG)神经元胞体增大受阻,表皮神经纤维分布明显减少,且对机械刺激的反应显著减弱,表明了PNS小胶质细胞在调控外周神经元发育与功能成熟过程中的重要作用。

图3. PNS microglia是外周神经元胞体变大,轴突生长,功能成熟所需要的
进化关联:PNS小胶质细胞丰度与物种体型/神经元胞体大小正相关
通过对24种脊椎动物(涵盖鱼类、两栖类、爬行类及哺乳类)进行系统演化分析,团队发现PNS小胶质细胞起源古老,在鱼类、两栖类和爬行类的背根神经节中就已存在。有趣的是,PNS小胶质细胞的丰度与物种的体型大小以及外周神经元胞体大小成正相关,即物种体型越大,外周神经元胞体越大,PNS小胶质细胞的丰度越高,而体型越小的物种,胞体越小,PNS 小胶质细胞越罕见或不存在。这也从侧面证明了PNS小胶质细胞具有调控神经元胞体生长的功能。

图4. PNS microglia在进化上古老且与物种体型/神经元胞体大小正相关
科学意义
PNS小胶质细胞的发现打破了过去一直认为的“小胶质细胞不存在于外周神经系统”的经典认知。该发现不仅提出了新的免疫-神经互作模式,也拓展了我们对小胶质细胞分布和功能的理解,有望为外周神经系统的发育以及疾病的发生发展研究提供新的视角。
通讯作者简介
李汉杰,国家杰青,重点研发计划首席科学家,中国科学院深圳先进技术研究院研究员。课题组采用“数据和假说双驱动”的研究范式,利用计算生物学,分子细胞生物学,临床样本和动物模型,深入探究人体免疫细胞在生理及病理状态下的发育分化与功能。以通讯或第一作者(含共同)发表多篇高水平论文,包括Cell 3篇(2025,2023,2019)、Cell Research(2020,2012)、Cell Reports Medicine(2024)、Cellular and Molecular Immunology、Cell Discovery、Cell Reports等期刊,总引用超4600次。成果入选2023年国内十大科技新闻(科技日报),2023年深圳市科技创新十件大事(深圳特区报)。曾荣获中组部“海外高层次人才青年项目”、欧盟“玛丽-居里奖学金”、德国“洪堡学者”。作为首席科学家,主持科技部重点研发计划“发育编程及其代谢调节”重点专项。
致谢与资助
中国科学院深圳先进技术研究院吴志生、王毅恒、陈巍魏、孙华及深圳市宝安区妇幼保健院陈晓燕博士为共同第一作者。感谢国家自然科学基金(32425024)、科技部重点研发计划(2020YFA0804100)、深圳市医学科学院专项基金(B2302006)等支持。
原文链接:https://doi.org/10.1016/j.cell.2025.02.007
课题组招聘
实验室长期招收计算生物学、分子细胞生物学、免疫学、基础医学研究员/研究生/博士后,欢迎有志之士前来咨询并加入我们的研究团队。
