学术动态
曾泽贤团队《Immunity》发文开发免疫相关功能基因组学分析平台ICRAFT揭示肿瘤免疫治疗双效靶点TNFAIP3
作者:曾泽贤 来源自:中国免疫学会 点击数:15887 发布时间:2025-03-28
近年来,免疫治疗(如PD-1/PD-L1免疫检查点抑制剂)在癌症治疗中取得了突破性进展,为许多患者带来了前所未有的生存获益。然而,尽管部分患者在治疗初期表现出良好反应,但大量临床数据显示,并非所有患者都能从中受益,且部分患者在接受治疗后会产生耐药性。更重要的是,许多肿瘤治疗策略往往只关注如何杀伤癌细胞,却忽略了其对免疫系统的影响,导致一些治疗在削弱肿瘤的同时,也损害了机体的抗癌免疫能力。因此,寻找对癌细胞和免疫细胞均具正向调控作用的“双效靶点”,成为肿瘤免疫治疗领域的重大需求。然而,大量靶点发现研究主要基于转录组数据的相关性分析,难以直接揭示基因对肿瘤微环境和免疫细胞的功能影响,这使得免疫治疗靶点的精准筛选尤为困难。
2025年2月28日,北京大学前沿交叉研究院曾泽贤研究员、清华大学基础医学院潘登研究员、北京大学人民医院高志冬副主任医师团队在《Immunity》期刊在线发表题为“Integrated computational analysis identifies therapeutic targets with dual action in cancer cells and T cells”的研究论文。该研究系统整合CRISPR筛选与多组学数据,开发了免疫相关功能基因靶点分析平台ICRAFT(Immune-related CRISPR screen Analyzer of Functional Targets),实现了对肿瘤免疫治疗“双效靶点”(dual-action targets)的高效识别与功能预测。

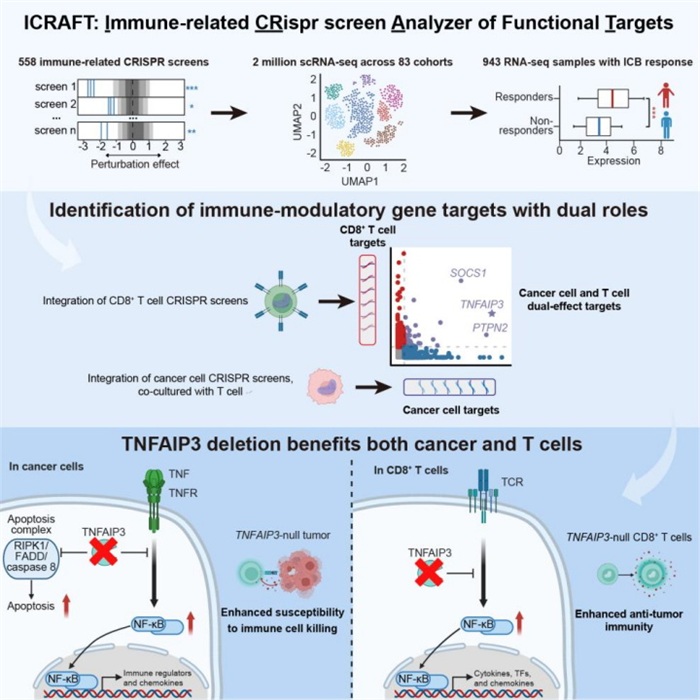
在这项研究中,研究团队开发的功能靶点分析平台ICRAFT整合了558项免疫相关CRISPR筛选实验结果、200万单细胞转录组数据及近千份免疫治疗临床前样本基因表达数据,为高效识别具有免疫调节功能的靶点提供了有力工具。
通过整合并对比不同细胞类型的CRISPR筛选数据,研究团队鉴定出82个在癌细胞和T细胞中均具有免疫调节作用的候选基因。其中,TNFAIP3的缺失能够在癌细胞中增强其对免疫细胞杀伤的敏感性,同时在T细胞中提升其免疫杀伤效应功能。该基因编码的A20蛋白是经典的TNF/NF-κB信号负调控因子,其功能缺失可分别促进癌细胞对TNF诱导的凋亡反应,并增强T细胞的活化状态及细胞因子的分泌能力。进一步的体内外实验证实,靶向TNFAIP3显著增强了抗肿瘤免疫反应,为开发作用于多个细胞类型、具协同效应的联合免疫治疗策略提供了新的可行路径与关键靶点。
值得注意的是,TNFAIP3也被广泛认为与系统性红斑狼疮、类风湿关节炎等自身免疫疾病密切相关。基于这一交叉特性,研究团队在文章结尾提出一个前瞻性的科学假设:尽管自身免疫反应常被视为导致组织损伤和炎症的病理过程,但在特定背景下,其激活可能反而对抑制肿瘤的发生和进展具有潜在保护效应。这一假说尚需通过系统性的实验研究与临床数据进一步验证,但对自身免疫调节机制与肿瘤免疫反应之间动态关系的探索,将为未来肿瘤精准免疫干预策略的优化提供新的理论基础和研究方向。
本研究为免疫治疗靶点的精准识别提供了强有力的技术平台和理论支撑。ICRAFT平台作为一个开放资源,自上线以来已被国内外研究人员广泛使用,访问量超过一万次,正在逐步发展成为肿瘤免疫学与功能基因组学领域的重要工具。
北京大学定量生物学中心2021级博士生罗策,北京大学-清华大学生命科学联合中心博士后张瑞和2022级博士生郭睿为该论文的共同第一作者。北京大学人民医院高志冬副教授、清华大学基础医学院潘登助理教授及北京大学定量生物学中心曾泽贤助理教授为本文的共同通讯作者。
原文链接:https://doi.org/10.1016/j.immuni.2025.02.007
2025年2月28日,北京大学前沿交叉研究院曾泽贤研究员、清华大学基础医学院潘登研究员、北京大学人民医院高志冬副主任医师团队在《Immunity》期刊在线发表题为“Integrated computational analysis identifies therapeutic targets with dual action in cancer cells and T cells”的研究论文。该研究系统整合CRISPR筛选与多组学数据,开发了免疫相关功能基因靶点分析平台ICRAFT(Immune-related CRISPR screen Analyzer of Functional Targets),实现了对肿瘤免疫治疗“双效靶点”(dual-action targets)的高效识别与功能预测。

在这项研究中,研究团队开发的功能靶点分析平台ICRAFT整合了558项免疫相关CRISPR筛选实验结果、200万单细胞转录组数据及近千份免疫治疗临床前样本基因表达数据,为高效识别具有免疫调节功能的靶点提供了有力工具。
通过整合并对比不同细胞类型的CRISPR筛选数据,研究团队鉴定出82个在癌细胞和T细胞中均具有免疫调节作用的候选基因。其中,TNFAIP3的缺失能够在癌细胞中增强其对免疫细胞杀伤的敏感性,同时在T细胞中提升其免疫杀伤效应功能。该基因编码的A20蛋白是经典的TNF/NF-κB信号负调控因子,其功能缺失可分别促进癌细胞对TNF诱导的凋亡反应,并增强T细胞的活化状态及细胞因子的分泌能力。进一步的体内外实验证实,靶向TNFAIP3显著增强了抗肿瘤免疫反应,为开发作用于多个细胞类型、具协同效应的联合免疫治疗策略提供了新的可行路径与关键靶点。

值得注意的是,TNFAIP3也被广泛认为与系统性红斑狼疮、类风湿关节炎等自身免疫疾病密切相关。基于这一交叉特性,研究团队在文章结尾提出一个前瞻性的科学假设:尽管自身免疫反应常被视为导致组织损伤和炎症的病理过程,但在特定背景下,其激活可能反而对抑制肿瘤的发生和进展具有潜在保护效应。这一假说尚需通过系统性的实验研究与临床数据进一步验证,但对自身免疫调节机制与肿瘤免疫反应之间动态关系的探索,将为未来肿瘤精准免疫干预策略的优化提供新的理论基础和研究方向。
本研究为免疫治疗靶点的精准识别提供了强有力的技术平台和理论支撑。ICRAFT平台作为一个开放资源,自上线以来已被国内外研究人员广泛使用,访问量超过一万次,正在逐步发展成为肿瘤免疫学与功能基因组学领域的重要工具。
北京大学定量生物学中心2021级博士生罗策,北京大学-清华大学生命科学联合中心博士后张瑞和2022级博士生郭睿为该论文的共同第一作者。北京大学人民医院高志冬副教授、清华大学基础医学院潘登助理教授及北京大学定量生物学中心曾泽贤助理教授为本文的共同通讯作者。
原文链接:https://doi.org/10.1016/j.immuni.2025.02.007
