学术动态
周洁团队《Immunity》发文揭示胆汁酸受体FXR通过诱导肠上皮细胞铁死亡促进新生期肠道炎症
作者:周洁 来源自:中国免疫学会 点击数:15303 发布时间:2025-03-24
坏死性小肠结肠炎(Necrotizing enterocolitis, NEC)是一种常见的新生儿科急性危重症,是因过度炎症引起的肠道缺血与组织坏死。NEC在极低体重新生儿(小于1500 g)中发病率约为7%,总死亡率长期维持在30%甚至更高。对于需要立即手术的患者,NEC的死亡率高达80%。NEC病因复杂,涉及遗传易感性、早产、和不适当喂养方式等。针对NEC的临床治疗,目前主要是对症治疗,包括停止肠内喂养、提供血流动力学支持及使用广谱抗生素。早产儿不成熟的肠黏膜屏障、菌群失调和肠上皮炎症信号过度激活在NEC的发生中发挥重要作用。但NEC的确切免疫病理机制尚待阐明。
2025年2月28日,天津医科大学周洁课题组在《Immunity》在线发表题为“Bile acid receptor FXR promotes intestinal epithelial ferroptosis and subsequent ILC3 dysfunction in neonatal necrotizing enterocolitis”的研究论文,这项研究揭示了NEC患者及其小鼠模型中,肠上皮细胞高表达胆汁酸受体FXR,上调的FXR通过靶向Acsl4促进肠上皮细胞发生铁死亡,随后释放的脂质过氧化物可通过抑制3型先天淋巴样细胞(ILC3s)的功能,从而加重NEC疾病。靶向肠道FXR或铁死亡可显著缓解小鼠NEC疾病症状。

这项研究中,团队首先利用高效液相色谱技术分析临床新生儿血浆样本,发现血浆FGF19(FXR下游靶蛋白)水平与新生儿成熟程度呈负相关,与肠道通透性和炎症指标呈正相关。进一步利用NEC患者的肠道组织免疫荧光、将NEC患者粪菌移植给乳鼠、FXR肠道特异性敲除小鼠等策略,证实新生期菌群紊乱可诱导肠道上皮细胞FXR过度激活,从而加重NEC疾病。
进一步利用肠上皮细胞的转录组测序及非靶向脂质代谢组学分析,发现FXR可促进肠上皮细胞发生铁死亡;进一步证明铁死亡关键分子Acsl4是FXR的下游直接靶基因。给予ACSL4抑制剂会显著拮抗由FXR激活所导致的肠上皮细胞铁死亡。在此基础上,探讨肠上皮细胞铁死亡如何参与NEC疾病的发生。肠道组织转录组测序提示:敲除FXR可上调肠道IL-22信号通路,给予IL-22中和抗体可拮抗FXR肠道特异性敲除小鼠对NEC疾病表型的缓解作用。进一步利用流式细胞术确定肠上皮细胞发生铁死亡后可抑制ILC3及其分泌IL-22的水平。通过体外ILC3与肠上皮细胞系Caco2萃取上清共培养实验, 确定发生铁死亡的肠道上皮,通过产生氧化型脂质抑制ILC3分泌IL-22。
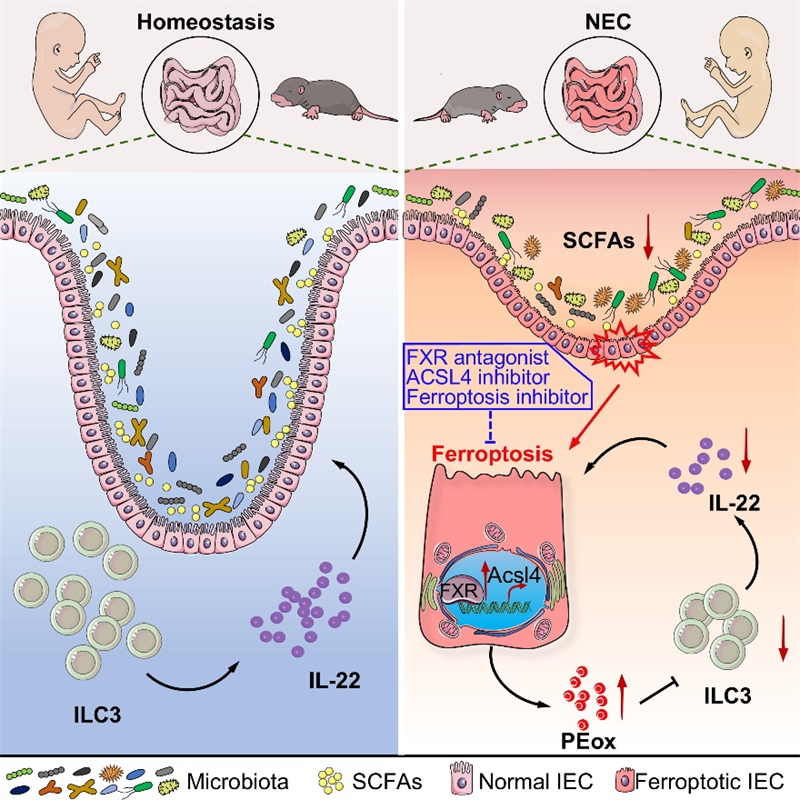
为探讨FXR介导的肠上皮细胞铁死亡在NEC疾病中的干预价值,给予野生型乳鼠肠道FXR拮抗剂、铁死亡抑制剂、ACSL4抑制剂,构建NEC模型并评估其生存率、肠道病理评分,肠道通透性以及促炎因子表达等疾病指标,证实靶向干预肠道FXR及铁死亡可显著缓解NEC疾病症状。最后通过对临床NEC患者血浆进行非靶向脂质代谢组学分析及组织免疫荧光染色,确定NEC患者肠道中氧化型脂质含量显著高于健康对照,且与患者疾病指标呈正相关。
以上研究结果揭示了出生后肠道菌群-肠上皮细胞-ILC3之间的互作在肠道稳态建立中的重要性,解析了生命早期菌群失调导致肠道炎症发生的免疫学机制,为NEC的免疫干预提供了新策略。
天津医科大学基础医学院/天津市免疫学研究所周洁教授为通讯作者,团队博士生张玉鑫、景宇超博士、何娟博士、博士生董睿为共同第一作者。
原文链接:https://doi.org/10.1016/j.immuni.2025.02.003
2025年2月28日,天津医科大学周洁课题组在《Immunity》在线发表题为“Bile acid receptor FXR promotes intestinal epithelial ferroptosis and subsequent ILC3 dysfunction in neonatal necrotizing enterocolitis”的研究论文,这项研究揭示了NEC患者及其小鼠模型中,肠上皮细胞高表达胆汁酸受体FXR,上调的FXR通过靶向Acsl4促进肠上皮细胞发生铁死亡,随后释放的脂质过氧化物可通过抑制3型先天淋巴样细胞(ILC3s)的功能,从而加重NEC疾病。靶向肠道FXR或铁死亡可显著缓解小鼠NEC疾病症状。

这项研究中,团队首先利用高效液相色谱技术分析临床新生儿血浆样本,发现血浆FGF19(FXR下游靶蛋白)水平与新生儿成熟程度呈负相关,与肠道通透性和炎症指标呈正相关。进一步利用NEC患者的肠道组织免疫荧光、将NEC患者粪菌移植给乳鼠、FXR肠道特异性敲除小鼠等策略,证实新生期菌群紊乱可诱导肠道上皮细胞FXR过度激活,从而加重NEC疾病。
进一步利用肠上皮细胞的转录组测序及非靶向脂质代谢组学分析,发现FXR可促进肠上皮细胞发生铁死亡;进一步证明铁死亡关键分子Acsl4是FXR的下游直接靶基因。给予ACSL4抑制剂会显著拮抗由FXR激活所导致的肠上皮细胞铁死亡。在此基础上,探讨肠上皮细胞铁死亡如何参与NEC疾病的发生。肠道组织转录组测序提示:敲除FXR可上调肠道IL-22信号通路,给予IL-22中和抗体可拮抗FXR肠道特异性敲除小鼠对NEC疾病表型的缓解作用。进一步利用流式细胞术确定肠上皮细胞发生铁死亡后可抑制ILC3及其分泌IL-22的水平。通过体外ILC3与肠上皮细胞系Caco2萃取上清共培养实验, 确定发生铁死亡的肠道上皮,通过产生氧化型脂质抑制ILC3分泌IL-22。

为探讨FXR介导的肠上皮细胞铁死亡在NEC疾病中的干预价值,给予野生型乳鼠肠道FXR拮抗剂、铁死亡抑制剂、ACSL4抑制剂,构建NEC模型并评估其生存率、肠道病理评分,肠道通透性以及促炎因子表达等疾病指标,证实靶向干预肠道FXR及铁死亡可显著缓解NEC疾病症状。最后通过对临床NEC患者血浆进行非靶向脂质代谢组学分析及组织免疫荧光染色,确定NEC患者肠道中氧化型脂质含量显著高于健康对照,且与患者疾病指标呈正相关。
以上研究结果揭示了出生后肠道菌群-肠上皮细胞-ILC3之间的互作在肠道稳态建立中的重要性,解析了生命早期菌群失调导致肠道炎症发生的免疫学机制,为NEC的免疫干预提供了新策略。
天津医科大学基础医学院/天津市免疫学研究所周洁教授为通讯作者,团队博士生张玉鑫、景宇超博士、何娟博士、博士生董睿为共同第一作者。
原文链接:https://doi.org/10.1016/j.immuni.2025.02.003
