学术动态
徐和平课题组发现脂滴可介导细胞间免疫信号传递并促进呼吸道过敏反应
作者:徐和平 来源自:中国免疫学会 点击数:10749 发布时间:2024-11-15
2024年11月12日,西湖大学徐和平课题组在《Immunity》杂志发表题为“Alarmin-loaded extracellular lipid droplets induce airway neutrophil infiltration during type 2 inflammation”的研究成果。该研究发现2型固有淋巴样细胞(group 2 innate lymphoid cell, ILC2)释放到细胞外的脂滴可以激活和招募中性粒细胞,进而促进呼吸道过敏性炎症反应。
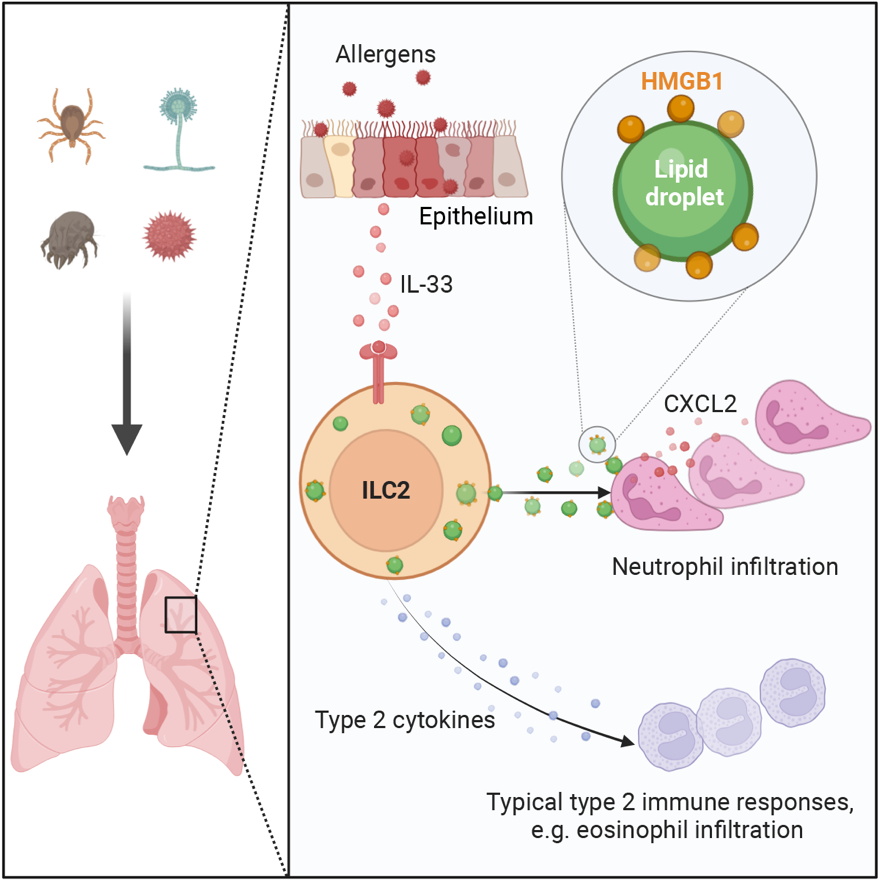
2型炎症反应是机体对寄生虫和其他胞外致病微生物的重要防御机制,同时也是维持机体各系统生理平衡的关键因素。然而,过度活跃的2型炎症反应又与过敏等慢性疾病紧密相关,这些慢性炎症疾病目前临床上缺乏有效的根治手段,严重影响患者生活质量,并对社会经济造成负担。近些年徐和平课题组与合作者致力于解析2型炎症反应的生理和病理功能以及相关调控机制(Xu et al, Immunity 2019; Cao et al, Immunity 2023; Zang et al, Immunity 2023; Li et al, Science 2023)。2型炎症反应的核心标志是白细胞介素(IL)-4、IL-5和IL-13等2型炎症细胞因子的产生。而ILC2作为近些年新发现的固有免疫细胞,是2型炎症反应的关键调控者。活化的ILC2通过大量分泌2型炎症细胞因子,激活下游效应细胞,从而促进2型炎症反应的进行。最典型的2型炎症效应细胞是嗜酸性粒细胞,在过敏性哮喘疾病患者的血液、痰液和气道中均能检测到嗜酸性粒细胞数目升高。但临床数据也显示,重度哮喘患者气道内中性粒细胞的增加同样显著。虽然与嗜酸性粒细胞同属粒细胞家族,但是中性粒细胞并非传统的2型炎性效应细胞,它们不会响应2型炎症细胞因子的刺激与招募。关于中性粒细胞是如何被特异性地招募至呼吸道进而参与过敏性炎症反应这一问题还未有明确答案。
为了研究上述问题,徐和平课题组首先利用不同免疫细胞缺陷型小鼠构建哮喘模型,发现ILC2的缺陷会导致中性粒细胞无法浸润呼吸道。进一步通过ILC2过继转移动物实验证明ILC2的存在会促进中性粒细胞浸润呼吸道。这些实验表明ILC2可招募中性粒细胞浸润呼吸道来参与过敏性炎症反应。为了探究ILC2招募中性粒细胞的分子机制,团队构建了ILC2培养上清诱导中性粒细胞迁移的体外实验模型,并与合作者开展生化与蛋白组学实验鉴定出警报素HMGB1是ILC2分泌的能够招募中性粒细胞的关键蛋白分子。
HMGB1是一种广泛表达的核蛋白,可作为DNA伴侣蛋白来维持染色体结构。在机体有炎症反应时,HMGB1可以被释放到细胞外来作为警报分子发挥作用。已知HMGB1可以在细胞死亡期间被动释放,也可以从活细胞中主动分泌。但是细胞主动分泌HMGB1的具体过程和分子机制尚未完全明确。徐和平团队发现ILC2分泌HMGB1依赖于炎症细胞因子IL-33的刺激。通过生物信息学分析发现IL-33特异性地在ILC2内诱导形成了一个有利于脂滴积累的基因表达特征,从而导致细胞内积累形成大量脂滴。另一方面,通过免疫共沉淀结合蛋白质谱方法鉴定出与HMGB1相互作用的蛋白包括了PLIN3、ACSL5和BSCL2等与脂滴形成相关的重要分子。进一步使用成像实验观察到HMGB1定位可在脂滴膜表面。更加有趣地是团队研究发现,ILC2培养上清以及过敏动物模型的肺泡换洗液中也含有大量脂滴,且脂滴膜表面含有HMGB1分子。利用化学小分子破坏胞外脂滴可显著降低ILC2培养上清招募中性粒细胞的功能。通过遗传学方法抑制ILC2内脂滴积累会降低细胞外脂滴以及HMGB1分子的含量,进而抑制ILC2招募中性粒细胞;而反向添加从野生型ILC2培养上清中纯化的脂滴可恢复其招募中性粒细胞的能力。以上结果说明ILC2来源的携带着HMBG1的脂滴促进了中性粒细胞浸润呼吸道。
徐和平课题组先前发表的研究成果揭示了细胞内脂滴可作为能量储备来支持ILC2的快速增殖,进而促进2型炎症反应(Zang et al, Immunity 2023)。而此次的新成果发现了ILC2可以把携带着HMGB1警报素分子的脂滴释放到细胞外环境。这些细胞外脂滴可有效激活和招募中性粒细胞浸润呼吸道,进而加重过敏性炎症反应。这一新发现拓展了我们对ILC2与中性粒细胞交互作用的认知,提出了独立于传统2型细胞因子介导的效应细胞招募机制之外的新免疫通讯途径;揭示了脂滴作为免疫细胞间信息传递的新载体,为中性粒细胞在哮喘呼吸道中大量积累提供了新的理论视角和干预靶点。
西湖大学徐和平研究员为论文通讯作者,助理研究员饶泽兵为本文第一作者。研究项目的推进得益于胡奇实验室(西湖大学)和李颜实验室(南京大学)的鼎力合作。本项目受到科技部重点研发计划、国家自然基金委、浙江省自然基金委、西湖实验室、以及西湖教育基金会的资助;项目实施过程中得到了西湖大学实验动物中心、流式平台、质谱平台、基因组学平台、成像平台以及超算平台的大力支持。
原文链接:https://www.cell.com/immunity/fulltext/S1074-7613(24)00445-X
课题组简介与招聘信息
西湖大学系统免疫学实验室致力于探究免疫细胞与组织微环境的互作机制与网络,重点关注脑膜、肠道等屏障组织中代谢以及神经系统信号对免疫稳态和炎症反应的调节作用,期望为最终实现具有组织器官特异性靶向的精准免疫治疗奠定理论基础。在国家自然基金委杰出青年项目、联合基金重点项目、科技部重点研发计划以及国家海外高层次人才项目等项目的支持下,实验室各项课题进展顺利。当前由于项目需要急需招聘博士后1名、科研助理2名。欢迎各位青年才俊加入我们,共同成长和发展!联系邮箱:xuheping@westlake.edu.cn。

2型炎症反应是机体对寄生虫和其他胞外致病微生物的重要防御机制,同时也是维持机体各系统生理平衡的关键因素。然而,过度活跃的2型炎症反应又与过敏等慢性疾病紧密相关,这些慢性炎症疾病目前临床上缺乏有效的根治手段,严重影响患者生活质量,并对社会经济造成负担。近些年徐和平课题组与合作者致力于解析2型炎症反应的生理和病理功能以及相关调控机制(Xu et al, Immunity 2019; Cao et al, Immunity 2023; Zang et al, Immunity 2023; Li et al, Science 2023)。2型炎症反应的核心标志是白细胞介素(IL)-4、IL-5和IL-13等2型炎症细胞因子的产生。而ILC2作为近些年新发现的固有免疫细胞,是2型炎症反应的关键调控者。活化的ILC2通过大量分泌2型炎症细胞因子,激活下游效应细胞,从而促进2型炎症反应的进行。最典型的2型炎症效应细胞是嗜酸性粒细胞,在过敏性哮喘疾病患者的血液、痰液和气道中均能检测到嗜酸性粒细胞数目升高。但临床数据也显示,重度哮喘患者气道内中性粒细胞的增加同样显著。虽然与嗜酸性粒细胞同属粒细胞家族,但是中性粒细胞并非传统的2型炎性效应细胞,它们不会响应2型炎症细胞因子的刺激与招募。关于中性粒细胞是如何被特异性地招募至呼吸道进而参与过敏性炎症反应这一问题还未有明确答案。
为了研究上述问题,徐和平课题组首先利用不同免疫细胞缺陷型小鼠构建哮喘模型,发现ILC2的缺陷会导致中性粒细胞无法浸润呼吸道。进一步通过ILC2过继转移动物实验证明ILC2的存在会促进中性粒细胞浸润呼吸道。这些实验表明ILC2可招募中性粒细胞浸润呼吸道来参与过敏性炎症反应。为了探究ILC2招募中性粒细胞的分子机制,团队构建了ILC2培养上清诱导中性粒细胞迁移的体外实验模型,并与合作者开展生化与蛋白组学实验鉴定出警报素HMGB1是ILC2分泌的能够招募中性粒细胞的关键蛋白分子。
HMGB1是一种广泛表达的核蛋白,可作为DNA伴侣蛋白来维持染色体结构。在机体有炎症反应时,HMGB1可以被释放到细胞外来作为警报分子发挥作用。已知HMGB1可以在细胞死亡期间被动释放,也可以从活细胞中主动分泌。但是细胞主动分泌HMGB1的具体过程和分子机制尚未完全明确。徐和平团队发现ILC2分泌HMGB1依赖于炎症细胞因子IL-33的刺激。通过生物信息学分析发现IL-33特异性地在ILC2内诱导形成了一个有利于脂滴积累的基因表达特征,从而导致细胞内积累形成大量脂滴。另一方面,通过免疫共沉淀结合蛋白质谱方法鉴定出与HMGB1相互作用的蛋白包括了PLIN3、ACSL5和BSCL2等与脂滴形成相关的重要分子。进一步使用成像实验观察到HMGB1定位可在脂滴膜表面。更加有趣地是团队研究发现,ILC2培养上清以及过敏动物模型的肺泡换洗液中也含有大量脂滴,且脂滴膜表面含有HMGB1分子。利用化学小分子破坏胞外脂滴可显著降低ILC2培养上清招募中性粒细胞的功能。通过遗传学方法抑制ILC2内脂滴积累会降低细胞外脂滴以及HMGB1分子的含量,进而抑制ILC2招募中性粒细胞;而反向添加从野生型ILC2培养上清中纯化的脂滴可恢复其招募中性粒细胞的能力。以上结果说明ILC2来源的携带着HMBG1的脂滴促进了中性粒细胞浸润呼吸道。
徐和平课题组先前发表的研究成果揭示了细胞内脂滴可作为能量储备来支持ILC2的快速增殖,进而促进2型炎症反应(Zang et al, Immunity 2023)。而此次的新成果发现了ILC2可以把携带着HMGB1警报素分子的脂滴释放到细胞外环境。这些细胞外脂滴可有效激活和招募中性粒细胞浸润呼吸道,进而加重过敏性炎症反应。这一新发现拓展了我们对ILC2与中性粒细胞交互作用的认知,提出了独立于传统2型细胞因子介导的效应细胞招募机制之外的新免疫通讯途径;揭示了脂滴作为免疫细胞间信息传递的新载体,为中性粒细胞在哮喘呼吸道中大量积累提供了新的理论视角和干预靶点。
西湖大学徐和平研究员为论文通讯作者,助理研究员饶泽兵为本文第一作者。研究项目的推进得益于胡奇实验室(西湖大学)和李颜实验室(南京大学)的鼎力合作。本项目受到科技部重点研发计划、国家自然基金委、浙江省自然基金委、西湖实验室、以及西湖教育基金会的资助;项目实施过程中得到了西湖大学实验动物中心、流式平台、质谱平台、基因组学平台、成像平台以及超算平台的大力支持。
原文链接:https://www.cell.com/immunity/fulltext/S1074-7613(24)00445-X
课题组简介与招聘信息
西湖大学系统免疫学实验室致力于探究免疫细胞与组织微环境的互作机制与网络,重点关注脑膜、肠道等屏障组织中代谢以及神经系统信号对免疫稳态和炎症反应的调节作用,期望为最终实现具有组织器官特异性靶向的精准免疫治疗奠定理论基础。在国家自然基金委杰出青年项目、联合基金重点项目、科技部重点研发计划以及国家海外高层次人才项目等项目的支持下,实验室各项课题进展顺利。当前由于项目需要急需招聘博士后1名、科研助理2名。欢迎各位青年才俊加入我们,共同成长和发展!联系邮箱:xuheping@westlake.edu.cn。
