学术动态
刘军团队揭示新冠病毒T细胞免疫逃逸特征和分子机制
作者:刘军 来源自:中国免疫学会 点击数:16904 发布时间:2025-02-24
T细胞免疫作为机体适应性免疫的第二只“手臂”,是机体适应性免疫中与抗体免疫并行且互作的重要组成,T细胞识别抗原表位的能力对于清除病毒感染至关重要。新冠变异如何影响人群白细胞抗原(HLA)限制性表位的T细胞免疫识别,以及T细胞免疫是否也是新冠病毒出现变异的驱动力,目前尚缺乏足够的科学数据。
2025年1月28日,中国疾病预防控制中心病毒病预防控制所刘军研究员、高福院士和赵迎泽副研究员,联合北京地坛医院宋蕊主任医师及石家庄第五医院周吉坤主任医师等,在《Nature Immunology》杂志上发表题为“T cell immunity evasion by SARS-CoV-2 JN.1 escapees targeting two cytotoxic T cell epitope hotspots”的研究成果。本研究基于对当前全球的主要流行新冠毒株JN.1变异株的免疫分析,首次揭示了在特定HLA限制下,SARS-CoV-2 T细胞表位的免疫逃逸现象及其背后的分子机制,同时还提出T细胞介导的免疫压力可能是SARS-CoV-2进化的重要驱动力之一。
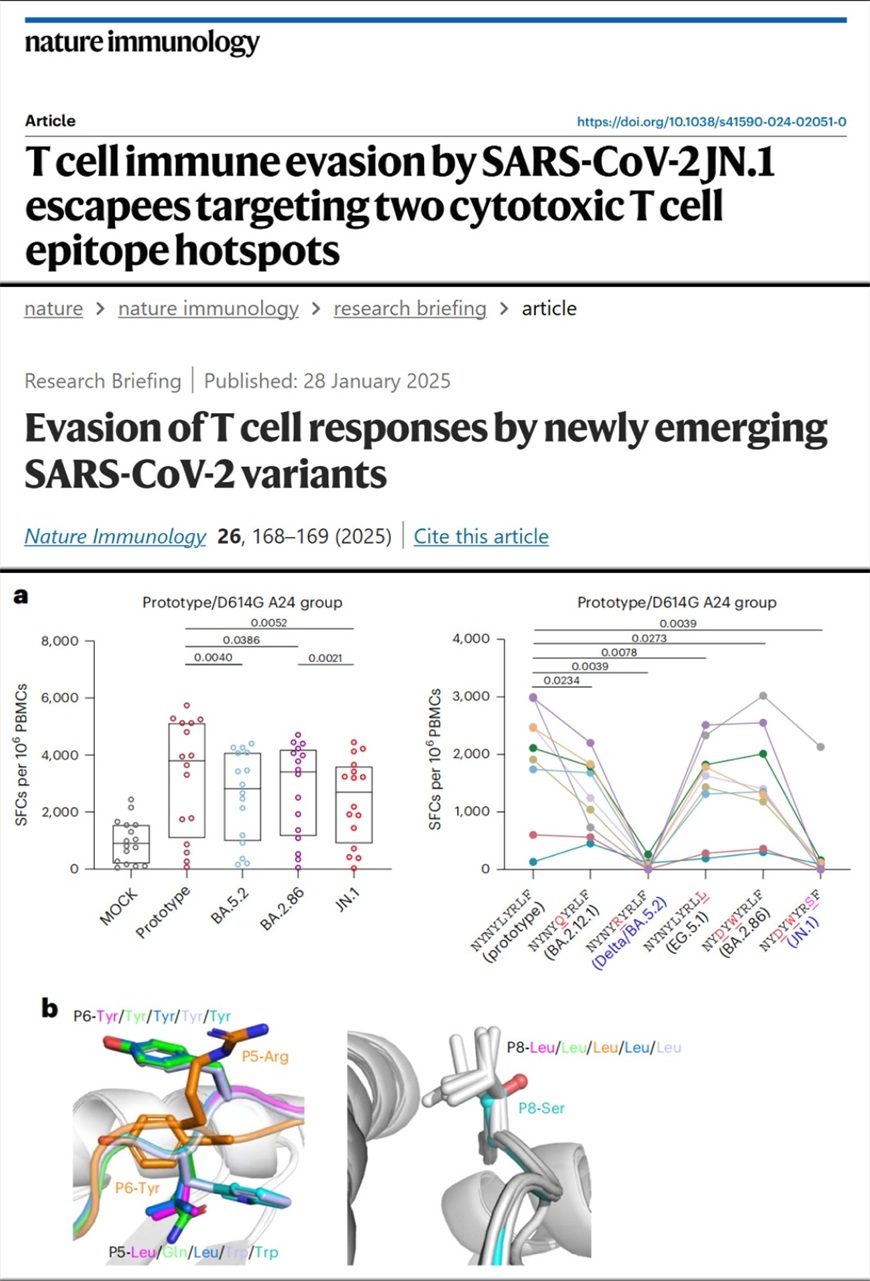
首先,研究团队设计合成了覆盖刺突蛋白(S)、膜蛋白(M)、核衣壳蛋白(N)及开放阅读框蛋白(ORF1ab)上JN.1变异株的特征变异位点所涉及的长多肽,以及HLA限制性CD8+表位短肽。通过团队前期建立的高灵敏度T细胞检测方法,检测了不同SARS-CoV-2毒株感染康复人群对多种新冠变异株的T细胞免疫,首次揭示了在特定人群HLA限制下,这些JN.1 T细胞表位的免疫逃逸特征,并发现HLA-A24人群与新冠T细胞免疫逃逸之间存在关联。
为进一步揭示T细胞免疫逃逸机制,研究团队聚焦于免疫显性优势表位HLA-A*2402–S448-456不同变体的T细胞交叉免疫反应和免疫逃逸特征,通过T细胞受体(TCR)体外结合及亲和力验证和结构免疫学分析,证实发生在该表位上的自然突变,如Delta/BA.5.2的L452R突变和JN.1的N450D/L452W/L455S复合突变,能够改变多肽的疏水性及影响T细胞受体识别从而诱导免疫逃逸。此外,研究团队还发现首次发生在N蛋白上高度保守区域的关键突变Q229K,能够诱导多个HLA-A2限制性表位的免疫逃逸现象。
综上所述,本研究系统性揭示了HLA限制性表位在T细胞免疫逃逸中的作用机制,为其他病原体的免疫逃逸研究提供了新思路,同时,该研究提出T细胞相关的免疫压力可能是新冠病毒进化的重要驱动力之一。这些发现为深入理解新冠病毒变异株的免疫逃逸策略提供了新的视角,也为未来疫苗设计和免疫策略优化提供了科学依据。
中国疾病预防控制中心病毒病预防控制所刘军研究员为最后通讯作者,高福院士、北京地坛医院宋蕊主任医师、石家庄第五医院周吉坤主任医师及病毒病所赵迎泽副研究员为共同通讯作者。课题组博士生田金珉、尚丙丽(温州医科大学)、张家宁、郭源源(山东大学)、李敏和胡月超为共同第一作者。该研究工作获得中国疾控中心传染病溯源预警与智能决策全国重点实验室的支持,以及国家重点研发计划和国家自然科学基金项目的资助。
原文链接:https://doi.org/10.1038/s41590-024-02051-0
2025年1月28日,中国疾病预防控制中心病毒病预防控制所刘军研究员、高福院士和赵迎泽副研究员,联合北京地坛医院宋蕊主任医师及石家庄第五医院周吉坤主任医师等,在《Nature Immunology》杂志上发表题为“T cell immunity evasion by SARS-CoV-2 JN.1 escapees targeting two cytotoxic T cell epitope hotspots”的研究成果。本研究基于对当前全球的主要流行新冠毒株JN.1变异株的免疫分析,首次揭示了在特定HLA限制下,SARS-CoV-2 T细胞表位的免疫逃逸现象及其背后的分子机制,同时还提出T细胞介导的免疫压力可能是SARS-CoV-2进化的重要驱动力之一。

首先,研究团队设计合成了覆盖刺突蛋白(S)、膜蛋白(M)、核衣壳蛋白(N)及开放阅读框蛋白(ORF1ab)上JN.1变异株的特征变异位点所涉及的长多肽,以及HLA限制性CD8+表位短肽。通过团队前期建立的高灵敏度T细胞检测方法,检测了不同SARS-CoV-2毒株感染康复人群对多种新冠变异株的T细胞免疫,首次揭示了在特定人群HLA限制下,这些JN.1 T细胞表位的免疫逃逸特征,并发现HLA-A24人群与新冠T细胞免疫逃逸之间存在关联。
为进一步揭示T细胞免疫逃逸机制,研究团队聚焦于免疫显性优势表位HLA-A*2402–S448-456不同变体的T细胞交叉免疫反应和免疫逃逸特征,通过T细胞受体(TCR)体外结合及亲和力验证和结构免疫学分析,证实发生在该表位上的自然突变,如Delta/BA.5.2的L452R突变和JN.1的N450D/L452W/L455S复合突变,能够改变多肽的疏水性及影响T细胞受体识别从而诱导免疫逃逸。此外,研究团队还发现首次发生在N蛋白上高度保守区域的关键突变Q229K,能够诱导多个HLA-A2限制性表位的免疫逃逸现象。
综上所述,本研究系统性揭示了HLA限制性表位在T细胞免疫逃逸中的作用机制,为其他病原体的免疫逃逸研究提供了新思路,同时,该研究提出T细胞相关的免疫压力可能是新冠病毒进化的重要驱动力之一。这些发现为深入理解新冠病毒变异株的免疫逃逸策略提供了新的视角,也为未来疫苗设计和免疫策略优化提供了科学依据。
中国疾病预防控制中心病毒病预防控制所刘军研究员为最后通讯作者,高福院士、北京地坛医院宋蕊主任医师、石家庄第五医院周吉坤主任医师及病毒病所赵迎泽副研究员为共同通讯作者。课题组博士生田金珉、尚丙丽(温州医科大学)、张家宁、郭源源(山东大学)、李敏和胡月超为共同第一作者。该研究工作获得中国疾控中心传染病溯源预警与智能决策全国重点实验室的支持,以及国家重点研发计划和国家自然科学基金项目的资助。
原文链接:https://doi.org/10.1038/s41590-024-02051-0
